Том 101, № 4 (2024)
- Год: 2024
- Статей: 11
- URL: https://journals.rcsi.science/0372-9311/issue/view/16959
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Геномный надзор за SARS-CoV-2 в Российской Федерации: возможности платформы VGARus
Аннотация
Введение. В ответ на пандемию COVID-19 в России были приняты комплексные меры реагирования. Одной из них стала разработка платформы агрегации вирусных геномов (VGARus) для мониторинга изменчивости вируса.
Цель работы — описать роль VGARus в отслеживании генетических изменений SARS-CoV-2.
Материалы и методы. Выравнивание вирусных геномов, последующую трансляцию в аминокислоты и поиск мутаций производили с помощью программы NextClade. С целью анализа геномной изменчивости подсчитывали число аминокислотных изменений относительно референсной последовательности.
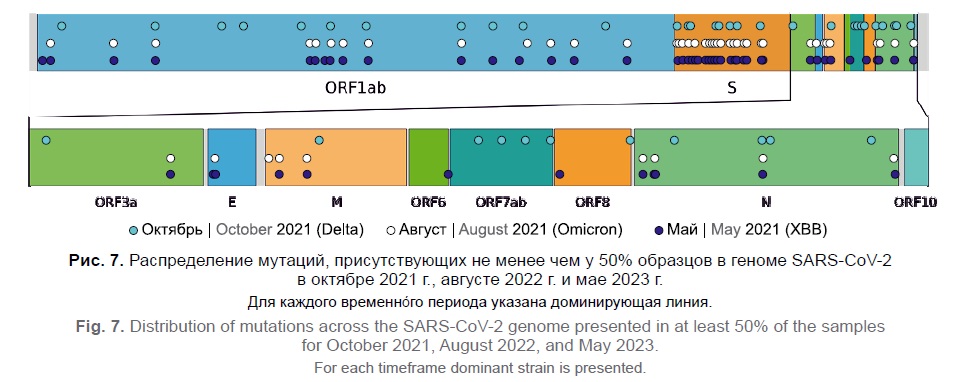
Результаты. Анализ данных VGARus позволил идентифицировать новые варианты вируса, что способствовало улучшению диагностических тестов и может помочь в разработке вакцин. Платформа предоставила возможность прогнозировать эпидемиологические тенденции и оперативно реагировать на изменения эпидемиологической ситуации. Например, с использованием VGARus был точно предсказан рост заболеваемости COVID-19 летом 2022 г. и в начале 2023 г., связанный с появлением субвариантов Omicron BA.5 и XBB. Данные платформы помогают проверять эффективность праймеров и ДНК-зондов, что обеспечивает высокую точность диагностики и снижает риск ложноотрицательных результатов.
Заключение. VGARus демонстрирует растущую роль геномного эпиднадзора в борьбе с COVID-19 и повышение готовности к будущим вспышкам инфекционных заболеваний. Платформа является мощным инструментом для формирования научно обоснованных решений по борьбе с пандемией и смягчению её последствий для здоровья населения, экономики и общества. Она предоставляет возможность оперативно получать информацию об эпидемиологической обстановке в конкретном регионе России, использовать геномные данные для проведения филогенетического анализа, сравнивать мутационный спектр последовательностей SARS-CoV-2 с зарубежными образцами. Данные VGARus позволяют проводить ретроспективный анализ и выдвигать гипотезы прогностического характера. Так, явно можно увидеть динамику смены различных вариантов вируса: последовательности, принадлежащие линиям Alpha, Beta, Delta, Omicron и многим менее распространённым, отчётливо формируют подъёмы заболеваемости, которые отражаются на эпидемиологической ситуации. В данный момент платформа расширяется для мониторинга изменчивости других патогенов, что увеличивает её значимость для общественного здравоохранения.
 435-447
435-447


Сибирская язва в Российской Федерации в 2023 году, или «старая сказка о главном»
Аннотация
Введение. Современная ситуация по сибирской язве (CЯ) в России характеризуется неустойчивостью. В 2023 г. отмечено увеличение числа вспышек инфекции по сравнению со средним многолетним показателем (за 5 лет).
Цель работы — оценка эпизоотолого-эпидемиологической ситуации по CЯ, сложившейся в России в 2023 г., и причин её ухудшения, анализ данных геномного эпидемиологического надзора за этой инфекцией.
Материалы и методы. Использовали информацию территориальных органов Роспотребнадзора о расследовании вспышек CЯ, справочные материалы о стационарно неблагополучных по CЯ пунктах и сибиреязвенных захоронениях. Филогенетическое положение идентифицированных штаммов Bacíllus anthracis и структуру геномов определяли на основе данных полногеномного секвенирования.
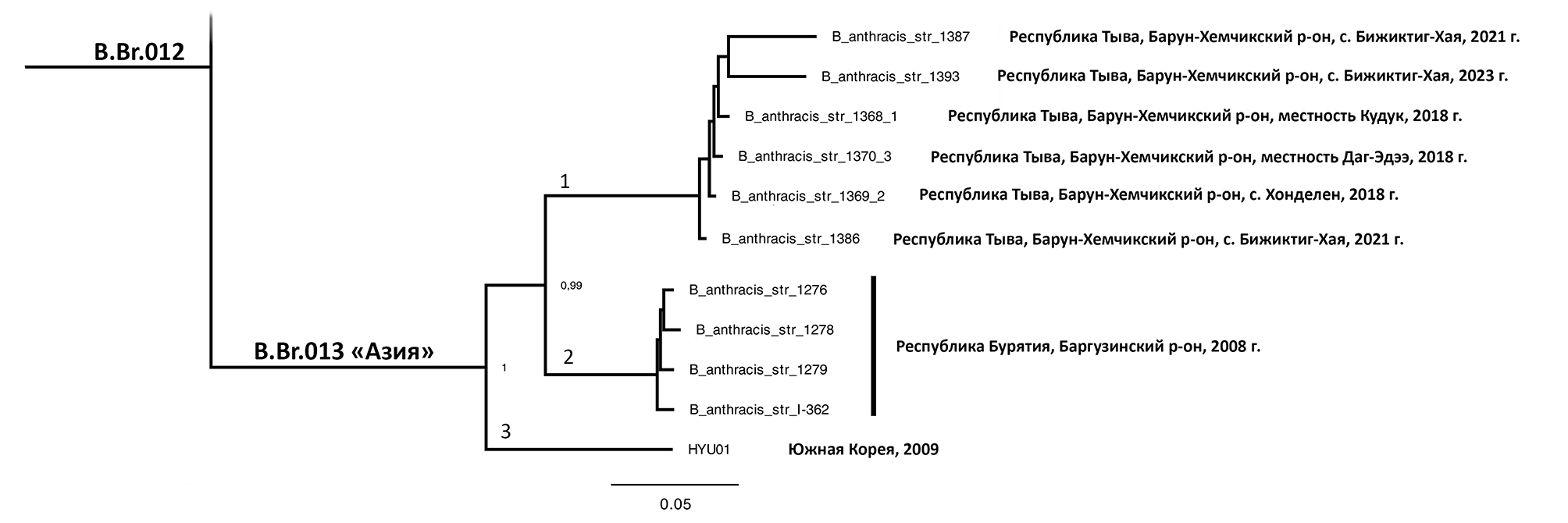
Результаты. В 2023 г. вспышки CЯ зарегистрированы в Чувашской Республике (1), Республике Тыва (1), Тамбовской (1), Рязанской (1) и Воронежской (3) областях. Заболело 14 сельскохозяйственных животных и 19 человек. Заражение животных, не вакцинированных против CЯ, а также привитых задолго до контакта с источником инфекции, происходило преимущественно при выпасе на территориях старых (неучтённых) почвенных очагов CЯ. Заболевание людей обусловлено контактом с больными животными при уходе, вынужденном убое, разделке, транспортировке туш и мяса, кулинарной обработке заражённого мяса и субпродуктов, употреблением в пищу недостаточно термически обработанного ливера. У 17 заболевших диагностирована кожная форма CЯ, у 2 — орофарингеальная форма в сочетании с кожной формой болезни. Во всех случаях установлена типичная для вида B. anthracis структура геномов. Показана филогенетическая связь изолятов со штаммами B. anthracis, ранее выделенными в России.
Заключение. Причиной неблагополучия по CЯ в 2023 г. стал ряд нарушений ветеринарного и санитарно- эпидемиологического нормирования на фоне наличия почвенных очагов инфекции. Стабилизация обстановки может быть достигнута только при постоянной реализации в полном объёме комплекса регламентированных профилактических мероприятий. Результаты молекулярно-генетического типирования штаммов B. anthracis, выделенных в ходе эпидемиологического расследования 7 вспышек СЯ на территории России в 2023 г., позволяют сделать вывод об их местном происхождении и типичной для вида структуре генома. Генетический анализ изолированных штаммов показал эффективность применения разработанной системы wgSNP-типирования при эпидемиологическом расследовании вспышек.
 448-461
448-461


Молекулярно-генетическая характеристика уропатогенных Escherichia coli, выделенных при бессимптомной бактериурии у беременных
Аннотация
Введение. Уропатогенные Escherichia coli (UPEC) являются доминирующими бактериальными патогенами при инфекциях мочевыводящих путей (ИМП). UPEC относятся к разным филогенетическим группам и обладают множеством факторов вирулентности, изучение которых в совокупности с оценкой их связи с клиническими формами ИМП необходимо для лучшего понимания патогенеза и разработки новых диагностических алгоритмов.
Цель исследования — молекулярно-генетическая характеристика UPEC, выделенных при бессимптомной бактериурии у беременных.
Материалы и методы. В исследование включены клинические изоляты E. coli (n = 70), выделенные у беременных с бессимптомной бактериурией (ББУ). Методом полимеразной цепной реакции определяли принадлежность к филогенетическим группам и 15 маркеров вирулентности — гены, ассоциированные с адгезией (fimH, papC, sfa, afa, focG), инвазией (ibeA), синтезом токсинов (cnf1, hlyA, sat, vat, usp), сидерофоров (fyuА, iroN, iuc), капсульного антигена (kpsМII). Для оценки статистической значимости различий средних величин применяли точный критерий Фишера. Статистически значимыми считали различия при 95% доверительном интервале (р < 0,05).
Результаты. Большинство изолятов UPEC, выделенных при ББУ, принадлежали к филогруппе В2 (51,4%) и характеризовались детекцией всех ассоциированных с UPEC факторов вирулентности, включённых в настоящее исследование; достоверно чаще были обнаружены гены, ассоциированные с адгезией (sfa, focG), синтезом токсинов (hlyA, cnf1, vat, usp) и капсул (kps), сидерофоры (fyuA, iroN, hlyA). Две и более детерминанты вирулентности выявлены у 93% изолятов.
Заключение. Определение ключевых детерминант вирулентности и/или комбинации генов вирулентности может быть прогностическим маркером для прогнозирования течения ИМП, особенно у беременных, и позволит расширить возможности диагностики с учётом вирулентных свойств уропатогена.
 462-469
462-469


Вирулентность и тканевая специфичность разных эпидемически значимых вариантов SARS-CoV-2 для золотистых сирийских хомячков
Аннотация
Введение. Животные модели инфекции SARS-CoV-2, воспроизводящие клинические особенности COVID-19 у человека, являются важными инструментами изучения патогенеза заболевания, трансмиссии возбудителя и незаменимы при испытаниях противовирусных лекарственных препаратов и вакцин.
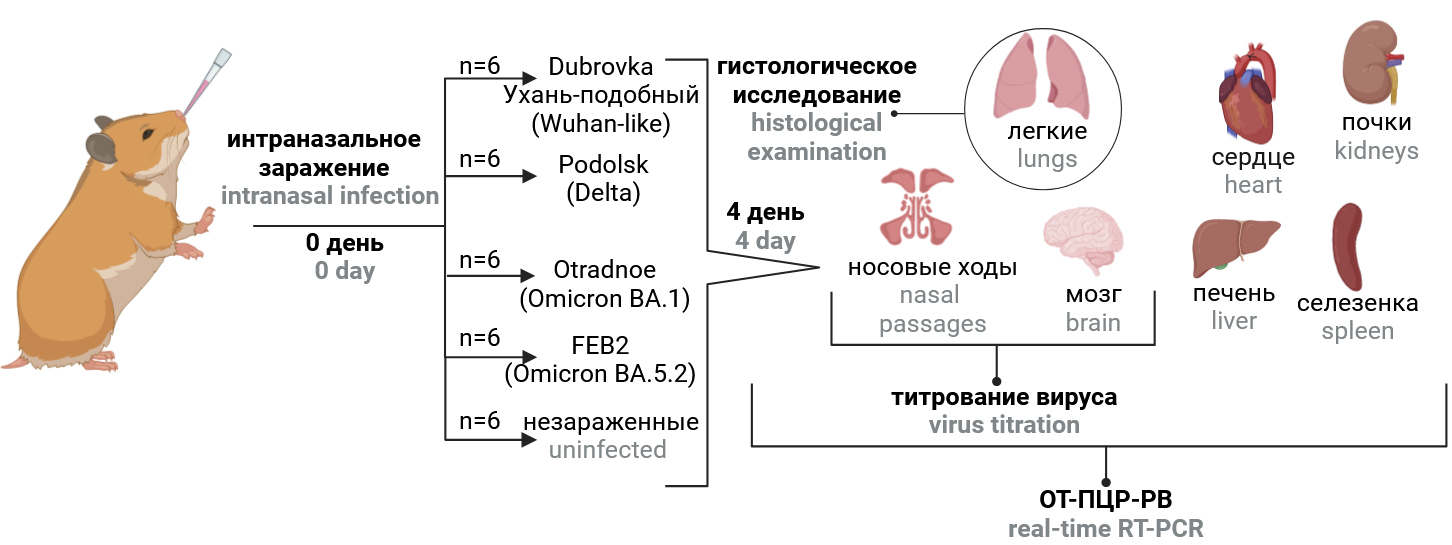
Целью исследования являлась оценка вирулентности и тканевой специфичности для золотистых сирийских хомячков штаммов SARS-CoV-2, относящихся к разным эпидемически значимым вариантам: Ухань-подобному, Delta, Omicron BA.1.1 и Omicron BA.5.2.
Материалы и методы. Хомячков интраназально заражали разными штаммами SARS-CoV-2. Вирулентность и тканевую специфичность штаммов SARS-CoV-2 оценивали путём сравнения динамики массы, вирусной нагрузки в органах и выраженности патоморфологических изменений в лёгких у заражённых и незаражённых животных.
Результаты. Наибольшей вирулентностью для хомячков обладал Ухань-подобный штамм, что проявлялось в развитии тяжёлой пневмонии и задержке в приросте массы на 14,6%, высоком содержании вируса в лёгких, носовых ходах и головном мозге — 6,2, 5,9 и 3,7 lg ТЦД50/мл гомогената соответственно. Предположительно именно поражение Ухань-подобным вирусом центральной нервной системы негативно повлияло на показатели массы и общее состояние животных. При заражении хомячков штаммами, относящимися к вариантам Delta и Omicron, незначительная потеря массы животными была неинформативной, поэтому при оценке патогенности вируса решающую роль играли такие показатели, как гистопатология лёгких, вирусная нагрузка в лёгких, носовых ходах, сердце и других органах. Особую ценность при сравнении тяжести пневмонии имела балльная оценка выраженности патоморфологических изменений в лёгких, поскольку она снижала субъективизм в оценке результатов гистологического исследования и давала полуколичественную оценку патологического процесса.
Заключение. Несмотря на выявленную более низкую вирулентность для хомячков штаммов, относящихся к вариантам Delta и Omicron, по сравнению с родоначальным Уханьским вирусом, данная животная модель COVID-19 сохраняет свою ценность для проведения доклинических испытаний противовирусных препаратов.
 470-482
470-482


Молекулярно-генетическая характеристика Streptococcus pneumoniae серогрупп 15 и 11, циркулирующих в России, и их связь с глобальными генетическими линиями
Аннотация
Цели исследования — генетический анализ Streptococcus pneumoniae серогрупп 15 и 11, циркулирующих в России, по параметрам: серотиповая принадлежность; клональный комплекс (СС); наличие детерминант резистентности и вирулентности; взаимосвязь с циркулирующими в мире генетическими линиями; наличие уникальных генов, значимых для проявления вирулентности; обоснование актуальных серотипов серогрупп 15 и 11 для включения в состав будущей конъюгированной вакцины.
Материалы и методы. В исследование включены полногеномные данные S. pneumoniae серогрупп 11 и 15.
Результаты. Российские геномы серогруппы 15 представлены в основном серотипами 15В и 15С, большинство относится к CC-1025, CC-1262. Для CC-1025 характерна более частая ассоциация с инвазивными заболеваниями. Представители СС-1025 и CC-1262 содержат уникальные для данных генетических линий, в пределах изучаемой популяции серогруппы 15, детерминанты вирулентности: транспортеры олигопептидов, фруктозоспецифичную фосфотрансферазную транспортную систему, уникальные варианты гидролаз, дополнительные транспортеры ионов железа, ген цинковой металлопротеазы ZmpC (активирующей матриксную металлопротеиназу 9 человека). Геномы серогруппы 11 представлены в основном серотипом 11А, большинство относится к СС-62 и СС-1012. К уникальным для СС-62 детерминантам вирулентности (в пределах изучаемой серогруппы 11) относятся бактериоцины, компоненты транспорта олигопептидов, флавинредуктазаподобный белок (адгезин, также защищает бактерии от окислительного стресса), оперон процессинга фукозы, PsaA (адгезин, также является компонентом АТФ-связывающего кассетного транспортера, импортирующего ионы марганца).
Выводы. В России среди невакцинных серогрупп распространены серогруппы 15 и 11. В геномах представителей этих серогрупп детерминант антимикробной резистентности не выявлено. Для каждой из распространённых в России генетических линий, ассоциированных с серогруппами 15 и 11, идентифицированы уникальные в пределах изучаемой серогруппы детерминанты вирулентности, которые могут способствовать успешности данных линий. В перспективные для России вакцины целесообразно включение серотипов 15B и 11A.
 483-501
483-501


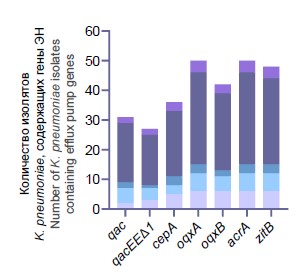
Распространённость генов qacEΔ1, qacE, oqxA, oqxB, acrA, cepA и zitB среди мультирезистентных Klebsiella pneumoniae, выделенных в кардиохирургическом стационаре
Аннотация
Актуальность. Инфекции, вызванные Klebsiella pneumoniae с множественной лекарственной устойчивостью (МЛУ), являются основной причиной смертности во всём мире. Широкое использование дезинфицирующих средств и антисептиков привело к появлению K. pneumoniae со сниженной чувствительностью к ним, что в сочетании с МЛУ может представлять существенную эпидемиологическую угрозу.
Целью исследования была оценка распространённости генов эффлюксных насосов и транспортёров, ассоциированных с устойчивостью к биоцидам, и их связи с резистентностью к антибиотикам среди изолятов K. pneumoniae, выделенных в кардиохирургическом стационаре.
Материалы и методы. Изоляты K. pneumoniae (n = 50), выделенные из клинического материала пациентов и смывов с медицинского оборудования, были проверены методом полимеразной цепной реакции на присутствие генов 4 типов эффлюксных насосов (qacEΔ1, qacE, oqxA, oqxB, acrA) и 2 транспортёров, участвующих в оттоке катионов (cepA) и ионов цинка (zitB). Для оценки силы ассоциации между генами устойчивости к биоцидам, генами бета-лактамаз и мобильных генетических элементов использовали тест ранговой корреляции Спирмена.
Результаты. Встречаемость K. pneumoniae, содержащих в геноме qacEΔ1, qacE, oqxA, oqxB, acrA, cepA и zitB, оказалась высокой: 54, 62, 100, 84, 100, 72 и 96% соответственно. Наиболее часто были обнаружены K. pneumoniae с комбинацией всех исследуемых насосов (32%), причём такие культуры были в 100% случаев мультирезистентными. Гены qacE, qacEΔ1 были тесно связаны с устойчивостью к цефалоспоринам, карбапенемам, фторхинолонам, генами карбапенемаз и интегронами. Среди клинических изолятов K. pneumoniae с МЛУ были широко представлены гены различных эффлюксных насосов, ассоциированных с устойчивостью к биоцидам, и их комбинации.
Заключение. Высокая распространённость генов эффлюксных насосов, ассоциированных с устойчивостью к четвертичным соединениям аммония, хлоргексидину и солям цинка, и их значимая связь с антибиотикорезистентностью у нозокомиальных K. pneumoniae подчёркивают важность дальнейшего изучения механизмов кросс-резистентности к биоцидам для совершенствования методов борьбы с патогенами с МЛУ.
 502-511
502-511


Оценка вклада симбиотических отношений микроорганизмов ротовой полости в развитие воспалительных изменений слизистой оболочки рта при полном отсутствии зубов
Аннотация
Введение. Фиксация на открытых поверхностях съёмных пластиночных протезов и мягких тканей ротовой полости бактерий в виде биоплёнки обеспечивает повышение вирулентности и резистентности микробного сообщества. Микроорганизмы, входящие в состав биоплёнки, зачастую находятся в симбиотических отношениях, что позволяет им увеличивать свой патогенный потенциал и вызывать развитие протезных стоматитов.
Цель исследования — оценка вклада симбиотических отношений бактерий ротовой полости в развитие воспалительных изменений слизистой оболочки рта при полном отсутствии зубов.
Материалы и методы. Сформированы две группы пациентов в возрасте 60–74 лет (82 мужчины и 49 женщин) с полным отсутствием зубов (К08.1), различающиеся по наличию клинических проявлений воспаления. Биологический материал, отобранный из ротовой полости пациентов, изучали с использованием культурального метода и полимеразной цепной реакции для выявления микроорганизмов полости рта. Для количественного выражения взаимодействия между членами микробиоценоза использовали коэффициент сходства Жаккара.
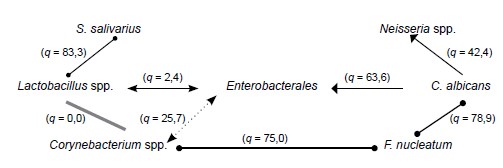
Результаты. У пациентов с полным отсутствием зубов в микробиоте протезного ложа доминировали коагулазоотрицательные и коагулазоположительные Staphylococcus spp., Neisseria spp., Candida spp., Fusobacterium spp. и представители порядка Enterobacterales. Установлены выраженные симбиотические связи между микроорганизмами порядка Enterobacterales, родов Lactobacillus, Neisseria и Corynebacterium, а также Streptococcus salivarius, C. albicans, F. nucleatum. При этом характер этих отношений зависел от наличия воспалительных изменений слизистой оболочки рта и, в свою очередь, влиял на развитие последних. Так, в отсутствие воспаления устойчивый синергизм проявляют Corynebacterium spp., Lactobacillus spp. и S. salivarius. В случае присоединения воспаления в ассоциации этих бактерий наблюдается внедрение F. nucleatum и вытеснение S. salivarius.
Заключение. Условно-патогенные микроорганизмы, формируя микробные ассоциации с разнонаправленными симбиотическими отношениями, могут увеличивать свою вирулентность, что, вероятно, позволяет им занимать свободные ниши в ротовой полости, а в последующем обеспечивать развитие патологического процесса воспалительного характера тканей протезного ложа.
 512-519
512-519


Сравнительный анализ структуры регуляторных генов штаммов Vibrio cholerae O1 биовара El Tor
Аннотация
Актуальность. Экспрессия генов ctxAB и tcpA-F, кодирующих основные факторы патогенности возбудителя холеры, контролируется регуляторными генами, структура которых в штаммах возбудителя, выделенных в разные годы текущей пандемии, изучена не в полной мере.
Цель работы — сравнительный анализ структуры регуляторных генов в штаммах Vibrio cholerae О1 биовара El Tor, изолированных на территории России и сопредельных стран на протяжении 7-й пандемии холеры.
Материалы и методы. Использовали нуклеотидные последовательности полных геномов 29 токсигенных штаммов, выделенных с 1970 по 2023 г. Анализ проводили с помощью программ «BioEdit v7.2.6.1» и «Blast».
Результаты. Проведён анализ 10 регуляторных генов (toxT, aphA, aphB, hns, hapR, vieA, luxO, luxT, carS, carR). Установлено, что практически у всех штаммов в гене hapR имеется вставка тимина в позиции 219. Исключение составил V. cholerae М3208 (Тамбов, 2023), у которого обнаружена вставка 5 нуклеотидов в данном гене. У 44,8% изученных штаммов выявлены мутации в гене luxO, функциональное значение которых не установлено. У 46,7 и 33,3% изученных геновариантов с аллелем ctxB1 обнаружены несинонимичные замены в генах hns (G319A) и vieA (C235T) соответственно. Все геноварианты с аллелем ctxB7 имеют гены hns и vieA с мутациями. Три геноварианта с аллелем ctxB7, завезённые в Россию в последние годы, содержат изменённую структуру гена carR (G265А).
Заключение. Структура генов (toxT, aphA, aphB, carS, luxT, hapR) является интактной у большинства изученных штаммов V. cholerae O1 El Tor. В то же время выявлена вариабельность генов hns (G319A), vieA (C235T) и carR (G256A). Мутации в данных генах могут быть использованы в качестве генетических меток современных геновариантов V. cholerae O1 El Tor.
 520-529
520-529


ОБЗОРЫ
Ограничения в создании искусственных популяций в агентном моделировании эпидемий: систематический обзор
Аннотация
Введение. Ключевым этапом агентного моделирования эпидемий, позволяющим исследователям учитывать индивидуальные особенности людей, является создание искусственной популяции. Основная сложность этой процедуры — поиск баланса между подробностью описания популяции и вычислительной эффективностью расчётов.
Цели и задачи обзора: критически проанализировать и обобщить актуальные данные о способах создания искусственных популяций; оценить ограничения и преимущества имеющихся подходов при решении различных задач в эпидемиологии.
Материалы и методы. Проведён анализ источников литературы, посвящённых агентному моделированию. Анализ сфокусирован на алгоритмах создания искусственной популяции с заданным уровнем детализации для моделирования респираторных инфекций человека.
Результаты. Обобщены подходы к созданию искусственных популяций. Выявлены основные принципы реализации взаимодействия между агентами: с помощью сетей контактов между агентами и на основе учёта перемещения агентов между локациями. Первый подход является наиболее эффективным для вычислений и простым; второй подход позволяет лучше учитывать изменение поведения агентов в ходе развития эпидемического процесса.
Заключение. Агентное моделирование — оптимальный инструмент при выборе наилучшего сценария проведения противоэпидемических мероприятий и исследовании роли индивидуальных особенностей людей в развитии эпидемий. При создании искусственной популяции важно включать в модель факторы, на которые может быть направлен контроль. Существенным ограничением является отсутствие фактологических данных о структуре популяции, однако его можно преодолеть за счёт привлечения косвенных данных.
 530-545
530-545


Роль Т-клеточного иммунитета важно учитывать при создании современных вакцин против клещевого энцефалита
Аннотация
Вирус клещевого энцефалита (КЭ) обладает высокой патогенностью, способен поражать центральную нервную систему, приводя к тяжелейшим хроническим последствиям либо летальному исходу. Единственной эффективной мерой борьбы с КЭ является профилактическая вакцинация. Используемые в настоящее время вакцины, полученные на основе инактивированного вируса КЭ, обеспечивают формирование протективного иммунного ответа, однако такие вакцины требуют многократного введения. Возможной причиной недолгосрочного иммунитета является формирование недостаточно напряжённого Т-клеточного ответа при использовании таких вакцин.
Цель обзора — анализ литературы, содержащей информацию о роли Т-клеточного иммунного ответа в защите организма от КЭ, о его значении для разработки вакцин, а также рассмотрение подходов к разработке новых вакцин против КЭ на основе различных платформ.
При подготовке обзора был проведён анализ литературы, представленной в базах PubMed, Scopus, Elsevier, Google Scholar по состоянию на апрель 2024 г. Для поиска использовали следующие ключевые слова: vaccine, tick-borne encephalitis virus, T-cell immune response, flaviviruses, вакцины, вирус клещевого энцефалита, Т-клеточный иммунный ответ, флавивирусы.
В ряде публикаций продемонстрировано, что структура Т-клеточного ответа при естественном заражении вирусом КЭ и после вакцинации инактивированным вирусом различна. В ходе вирусной инфекции активируются CD4+-Т-клетки как Th1-, так и Th2-типа, а также CD8+-Т-клетки, играющие важную роль в элиминации вирусной инфекции. После вакцинации преобладает ответ CD4+-Т-клеток по Th2-типу, что может являться причиной недолговечного иммунного ответа.
На сегодняшний день исследуется ряд различных типов экспериментальных вакцин против КЭ, таких как вакцины на основе живых аттенуированных вирусов, вакцины на основе вирусных векторов, вирусоподобные частицы, субъединичные вакцины, ДНК- и мРНК-вакцины, полиэпитопные иммуногены. В плане активации Т-клеточного ответа наиболее перспективными выглядят вакцины на основе Т-клеточных полиэпитопных иммуногенов, доставляемых в форме ДНК или мРНК.
 546-559
546-559


Оценка современного состояния фармацевтической разработки противостафилококковых профилактических препаратов
Аннотация
Инфекция, вызванная Staphylococcus aureus, является самой распространённой, приводящей к развитию серьёзных осложнений у человека. S. aureus относится к высоколетальным патогенам при бактериемии со смертностью примерно 18% в благополучных странах и до 27% — в развивающихся.
Одним из самых поразительных и сложных аспектов клинических проявлений, вызванных S. aureus, считается способность бактерии вырабатывать устойчивость к антибиотикам. Своевременной необходимостью является разработка альтернативных способов лечения стафилококковой инфекции. Перспективным направлением следует рассматривать применение иммунотерапии и иммунопрофилактики для активации противоинфекционного иммунного ответа у пациентов.
Цель обзора — анализ основных тенденций в разработке вакцин, направленных на профилактику инфекций, вызываемых S. aureus, и факторов вирулентности S. aureus.
В обзоре рассмотрены проводимые в последние годы разработки лекарственных препаратов, направленные на профилактику и лечение инфекций, вызываемых S. aureus. Особое внимание уделяется факторам патогенности (капсула, поверхностные белки и ферменты), которые могут быть полезны для создания новых вакцин-кандидатов или иммунных терапевтических средств. За последние годы проведение многочисленных клинических исследований кандидатов-вакцин, созданных на основе различных антигенов, с учётом особо значимых факторов патогенности стафилококка, оказывающих влияние на заболеваемость, не увенчались успехом из-за их низкой эффективности или недостаточно обоснованной безопасности (развитие нежелательных явлений). Одним из важнейших факторов, сдерживающих разработку вакцины, является отсутствие успешной трансляции протективности вакцины, которая наблюдается в доклинических исследованиях на экспериментальных моделях, но не подтверждается в клинических исследованиях.
Таким образом, по мнению многочисленных исследователей, необходимо рассматривать использование в составе вакцин несколько антигенов, сосредоточив внимание на различных механизмах патогенности S. aureus, включая использование адъювантов.
 560-572
560-572