Rare localization of avascular necrosis during treatment of COVID-19 with glucocorticosteroids
- Authors: Gonchar A.P.1, Blokhin I.A.1, Shumskaya Y.F.1,2
-
Affiliations:
- Research and Practical Clinical Center for Diagnostics and Telemedicine Technologies
- The First Sechenov Moscow State Medical University (Sechenov University)
- Issue: Vol 3, No 4 (2022)
- Pages: 384-392
- Section: Case reports
- URL: https://journals.rcsi.science/DD/article/view/146867
- DOI: https://doi.org/10.17816/DD110718
- ID: 146867
Cite item
Abstract
The development of bony avascular necrosis induced by glucocorticoid treatment of COVID-19 is a common adverse effect, with femoral head being the most commonly affected. Timely detection of avascular necrosis is important in the prevention of osteoarthrosis and other complications.
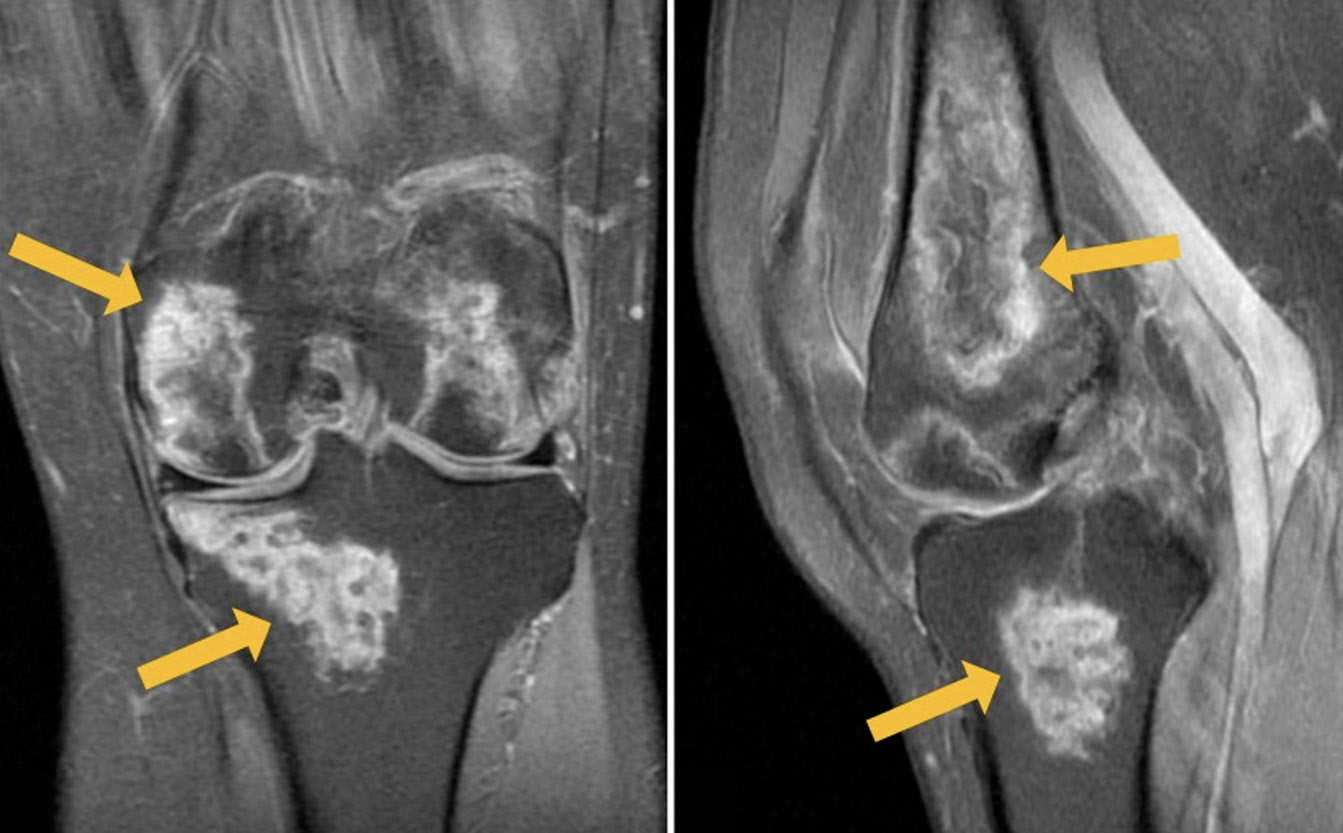
We present a clinical case of a 54-year-old patient hospitalized for novel coronavirus infection with complaints of severe pain in both knees 2 weeks after the disease onset. Magnetic resonance imaging revealed pronounced changes in both knees, corresponding to avascular necrosis. The results of conservative therapy, including non-steroidal anti-inflammatory drugs and bisphosphonate bone resorption inhibitors, produced a pronounced positive result. At follow-up examination 3 months later, there was no pain, but the knee joints still had slight restrictions of movement. Magnetic resonance imaging showed a significant decrease in the previously detected changes.
The side effects of glucocorticoids (impaired glucose tolerance, increased blood pressure, tachycardia, gastrointestinal erosive ulcers, sleep disorders, etc.) are widely known, but knee osteonecrosis caused by steroid intake rarely comes to the attention of clinicians. This clinical case emphasizes the complex nature of osteonecrosis pathogenesis and demonstrates a wide range of complications in corticosteroid therapy.
Full Text
##article.viewOnOriginalSite##About the authors
Anna P. Gonchar
Research and Practical Clinical Center for Diagnostics and Telemedicine Technologies
Email: a.gonchar@npcmr.ru
ORCID iD: 0000-0001-5161-6540
SPIN-code: 3513-9531
Russian Federation, Moscow
Ivan A. Blokhin
Research and Practical Clinical Center for Diagnostics and Telemedicine Technologies
Email: i.blokhin@npcmr.ru
ORCID iD: 0000-0002-2681-9378
SPIN-code: 3306-1387
Russian Federation, Moscow
Yuliya F. Shumskaya
Research and Practical Clinical Center for Diagnostics and Telemedicine Technologies; The First Sechenov Moscow State Medical University (Sechenov University)
Author for correspondence.
Email: yu.shumskaia@npcmr.ru
ORCID iD: 0000-0002-8521-4045
SPIN-code: 3164-5518
Russian Federation, Moscow; Moscow
References
- Temporary guidelines «Prevention, diagnosis and treatment of new coronavirus infection (COVID-19)». Version 3 (March 3, 2020) (approved by the Ministry of Health of the Russian Federation). (In Russ). Available from: https://www.garant.ru/products/ipo/prime/doc/73647088/. Accessed: 15.07.2022.
- Ali RS, Al-Sudani H, Tan IJ. Osteonecrosis of bilateral distal femurs in a pregnant patient following antenatal betamethasone. Cureus. 2022;14(3):e22735. doi: 10.7759/cureus.22735
- Zhang S, Wang C, Shi L, Xue Q. Beware of steroid-induced avascular necrosis of the femoral head in the treatment of COVID-19-experience and lessons from the SARS epidemic. Drug Des Devel Ther. 2021;15:983–995. doi: 10.2147/DDDT.S298691
- Agarwala SR, Vijayvargiya M, Pandey P. Avascular necrosis as a part of ‘long COVID-19’. BMJ Case Rep. 2021;14(7):e242101. doi: 10.1136/bcr-2021-242101
- Takao M, Sugano N, Nishii T, et al. Spontaneous regression of steroid-related osteonecrosis of the knee. Clin Orthop Relat Res. 2006;452:210–215. doi: 10.1097/01.blo.0000229278.51323.08
- Hines JT, Jo WL, Cui Q, et al. Osteonecrosis of the femoral head: an updated review of arco on pathogenesis, staging and treatment. J Korean Med Sci. 2021;36(24):e177. doi: 10.3346/jkms.2021.36.e177
- Disser NP, De Micheli AJ, Schonk MM, et al. Musculoskeletal consequences of COVID-19. J Bone Joint Surg Am. 2020;102(14):1197–1204. doi: 10.2106/JBJS.20.00847
- Karim AR, Cherian JJ, Jauregui JJ, et al. Osteonecrosis of the knee: review. Ann Transl Med. 2015;3(1):6. doi: 10.3978/j.issn.2305-5839.2014.11.13
- Patel MS, Gutman MJ, Abboud JA. Orthopaedic considerations following COVID-19: lessons from the 2003 SARS outbreak. JBJS Rev. 2020;8(7):e2000052. doi: 10.2106/JBJS.RVW.20.00052
- Kerachian MA, Séguin C, Harvey EJ. Glucocorticoids in osteonecrosis of the femoral head: a new understanding of the mechanisms of action. J Steroid Biochem Mol Biol. 2009;114(3-5):121–128. doi: 10.1016/j.jsbmb.2009.02.007
- Chan KL, Mok CC. Glucocorticoid-induced avascular bone necrosis: diagnosis and management. Open Orthop J. 2012;6:449–457. doi: 10.2174/1874325001206010449
- Powell C, Chang C, Naguwa SM, et al. Steroid induced osteonecrosis: an analysis of steroid dosing risk. Autoimmun Rev. 2010;9(11):721–743. doi: 10.1016/j.autrev.2010.06.007
- Takeda H, Nishise S, Fujishima S, et al. Osteonecrosis of the lateral femoral condyle in a patient with ulcerative colitis: report of a case. Clin J Gastroenterol. 2008;1(3):93–96. doi: 10.1007/s12328-008-0015-2
- Agarwala SR, Vijayvargiya M, Sawant T. Secondary osteonecrosis of the knee as a part of long COVID-19 syndrome: a case series. BMJ Case Rep. 2022;15(3):e248583. doi: 10.1136/bcr-2021-248583
- Angulo-Ardoy M, Ureña-Aguilera Á. Knee osteonecrosis after COVID-19. Fam Pract. 2021;38(Suppl 1):i45–i47. doi: 10.1093/fampra/cmab063
- Sulewski A, Sieroń D, Szyluk K, et al. Avascular necrosis bone complication after active COVID-19 infection: preliminary results. Medicina (Kaunas). 2021;57(12):1311. doi: 10.3390/medicina57121311
- Li W, Huang Z, Tan B, et al. General recommendation for assessment and management on the risk of glucocorticoid-induced osteonecrosis in patients with COVID-19. J Orthop Translat. 2021;31:1–9. doi: 10.1016/j.jot.2021.09.005
- Mont MA, Baumgarten KM, Rifai A, et al. Atraumatic osteonecrosis of the knee. J Bone Joint Surg Am. 2000;82(9):1279–1290. doi: 10.2106/00004623-200009000-00008
- Agarwala S, Sharoff L, Jagani N. Effect of zoledronic acid and alendronate on bone edema and pain in spontaneous osteonecrosis of the knee: a new paradigm in the medical management. Rev Bras Ortop (Sao Paulo). 2020;55(5):543–550. doi: 10.1016/j.rboe.2017.12.008
- Jureus J, Lindstrand A, Geijer M, et al. Treatment of spontaneous osteonecrosis of the knee (SPONK) by a bisphosphonate. Acta Orthop. 2012;83(5):511–514. doi: 10.3109/17453674.2012.729184
Supplementary files