Vol 65, No 4 (2020)
REVIEWS
The potential of synthetic small interfering RNA-based antiviral drugs for influenza treatment
Abstract
Influenza is a worldwide public health problem. Annually, this infection affects up to 15% of the world population; and about half a million people die from this disease every year. Moreover, influenza A and B viruses tend to garner most of the attention, as these types are a major cause of the epidemics and pandemics. Although the influenza virus primarily affects the respiratory tract, it may also affect the cardiovascular and central nervous systems. Several antiviral drugs, that target various stages of viral reproduction, have been considered effective for the treatment and prevention of influenza, but some virus strains become resistant to these medications. Thus, new strategies and techniques should be developed to overcome the antiviral drug resistance. Recent studies suggest that new drugs based on RNA interference (RNAi) appear to be a promising therapeutic approach that regulates the activity of viral or cellular genes. As it is known, the RNAi is a eukaryotic gene regulatory mechanism that can be triggered by a foreign double-stranded RNA (dsRNA) and results in the cleavage of the target messenger RNA (mRNA). This review discusses the prospects, advantages, and disadvantages of using RNAi in carrying out a specific treatment for influenza infection. However, some viruses confer resistance to small interfering RNAs (siRNA) targeting viral genes. This problem can significantly reduce the effectiveness of RNAi. Therefore, applying siRNAs targeting host cell factors required for influenza virus reproduction can be a way to overcome the antiviral drug resistance.
 182-190
182-190


Epstein-Barr virus (Herpesviridae: Gammaherpesvirinae: Lymphocryptovirus: Human gammaherpesvirus 4): replication strategies
Abstract
The Epstein-Barr virus (EBV), one of the most common in the human population, is capable of lifelong persistence in resting memory B-cells, in T-cells in case of type 2 EBV, and in some undifferentiated epithelial cells. In most people, EBV persistence is not accompanied by significant symptoms, but frequent virus activations are associated with the increased risks of severe diseases, such as chronic active Epstein-Barr virus infection, hemophagocytic lymphohistiocytosis, multiple sclerosis, systemic lupus erythematosus, gastric and nasopharyngeal carcinomas, and a variety of T- and B-cell lymphomas. Therefore, the molecular viral and host cell processes during asymptomatic or low-symptom EBV persistence are of great interest. This review describes the behavior of the viral DNA in an infected cell and the forms of its existence (linear, circular episome, chromosomally integrated forms), as well as methods of EBV genome copying. Two closely related cycles of viral reproduction are considered. Lytic activation is unfavorable for the survival of a particular viral genome in the cell, and may be a result of differentiation of a latently infected cell, or the arrival of stress signals due to adverse extracellular conditions. The EBV has a large number of adaptive mechanisms for limiting lytic reactivation and reducing hostility of host immune cells. Understanding the molecular aspects of EBV persistence will help in the future develop more effective targeted drugs for the treatment of both viral infection and associated diseases.
 191-202
191-202


ORIGINAL RESEARCHES
Patterns of the SARS-CoV-2 epidemic spread in a megacity
Abstract
The purpose of the study is to analyze patterns demonstrated by the COVID-19 epidemic process in a megacity during the increase, stabilization and reduction in the incidence, and to evaluate the effectiveness of the epidemic prevention measures.
Materials and methods. The comprehensive study incorporating epidemiological, molecular genetic and statistical research methods was conducted to analyze the spread of SARS-CoV-2 in Moscow during the COVID- 19 pandemic.
Results and discussion. It was found that the exponential growth in COVID-19 cases was prevented due to the most stringent control and restrictive measures deployed in Moscow to break the chains of SARS-CoV-2 transmission and due to people who were very disciplined in complying with the self-isolation rules. The analysis of the dynamics in detection of new COVID-19 cases showed that in a megacity, the impact of social distancing and self-isolation would become apparent only after 3.5 incubation periods, where the maximum length of the period is 14 days. It was discovered that the detection frequency of SARS-CoV-2 RNA in relatively healthy population and its dynamics are important monitoring parameters, especially during the increase and stabilization in the COVID-19 incidence, and are instrumental in predicting the development of the epidemic situation within a range of 1–2 incubation periods (14–28 days). In Moscow, the case fatality rate was 1.73% over the observation period (6/3/2020–23/6/2020).
Conclusion. The epidemiological analysis of the COVID-19 situation in Moscow showed certain patterns of the SARS-CoV-2 spread and helped evaluate the effectiveness of the epidemic prevention measures aimed at breaking the routes of transmission of the pathogen.
 203-211
203-211


Development of inactivated cultural yellow fever vaccine
Abstract
Introduction. The only currently available live vaccine against yellow fever (YF) based on chicken embryos infected with an attenuated 17D strain of the YF virus is one of the most effective vaccine preparations. However, the live vaccine is associated with “viscerotropic syndrome” (approximately 0.4 cases per 100 000 vaccinated). Therefore, the development and introduction of highly purified inactivated vaccine against YF is intended to ensure the maximum safety of vaccination against one of the most common human viral diseases.
Goals and objectives. Development and evaluation of immunogenicity of the cultural inactivated vaccine against YF at the laboratory model level.
Material and methods. Adaptation of 17D strain of YF virus to Vero cell culture, cultivation, removal of cellular DNA, inactivation with β-propiolactone, concentration, chromatographic purification, determination of protein and antigen of YF virus, assessment of immunogenicity in mice in parallel with commercial live vaccine.
Results and discussion. Immunogenicity: the determination of specific antibodies of class G (IgG) and virus neutralizing antibodies in the sera of immunized mice showed high level of antibodies exceeding that of immunized with commercial live vaccine. The optimal dose of antigen in the vaccine (total protein) was 50 μg/ml (5 μg/0.1 ml -dose and volume per 1 vaccination of mice). Thus, the laboratory version of cultural inactivated vaccine against YF is as effective (and even superior) as the commercial live vaccine.
Conclusion. Laboratory version of cultural inactivated vaccine against YF, which is not inferior in immunogenicity (in animal model) to commercial live vaccine, has been developed.
 212-217
212-217


Seroprevalence of hepatitis E virus (Hepeviridae: Orthohepevirus: Orthohepevirus A) among pregnant women in the highly endemic region of Kyrgyzstan
Abstract
Introduction. Hepatitis E (HE) is an important public health problem worldwide and is especially significant for pregnant women, among whom the associated mortality rate reaches 25%. The distribution of HE serological markers in this cohort in the endemic regions of Central Asia is poorly understood. The aim of the study was to assess the seroprevalence of HEV among pregnant women in the region of Kyrgyzstan where an increased incidence of HE is reported.
Material and methods. Blood serum of pregnant women, obtained from medical institutions in Bishkek, city of Osh and Osh region in the period from September 2016 to October 2019, and the control group of clinically healthy women were tested using the test systems “DS-IFA-ANTI-HEV-G” and “DS-IFA-ANTI-HEV-M” (NPO “Diagnostic Systems”, Russia).
Results. IgG antibodies to HEV were detected in 87 (5.9%) of 1472 examined pregnant women, IgM antibodies -in 64 (4.8%) of 1378, while 5 (0.34%) samples were simultaneously positive for IgG and IgM antibodies. The rates of detection of antibodies to HEV in women of three age categories from 17 to 36 years old in the studied and control groups were similar. The analysis of the seasonal dynamics of HEV seroprevalence in pregnant women in the period from February to September 2019 showed a tendency towards an increase in the values of the positivity coefficient of specific IgM antibodies by the beginning of the autumn. Antibodies to HEV were detected with highest frequency in women from Osh region.
Conclusions. A high risk of HEV infection for pregnant women in the surveyed region had been shown.
 218-227
218-227


TO VIROLOGIST’S AID
Study of the antiviral activity of the liquid corneal storage medium in relation to the herpes simplex virus in vitro
Abstract
The aim of the study was to assess the antiviral activity of the 7 types of liquid corneal storage medium on an experimental model of herpesvirus infection in vitro.
Material and methods. The study of antiviral activity of 7 samples of liquid corneal storage medium on a model of herpesvirus infection caused by the herpes simplex virus type 1 in Vero-cell using virological and statistical research methods was carried out.
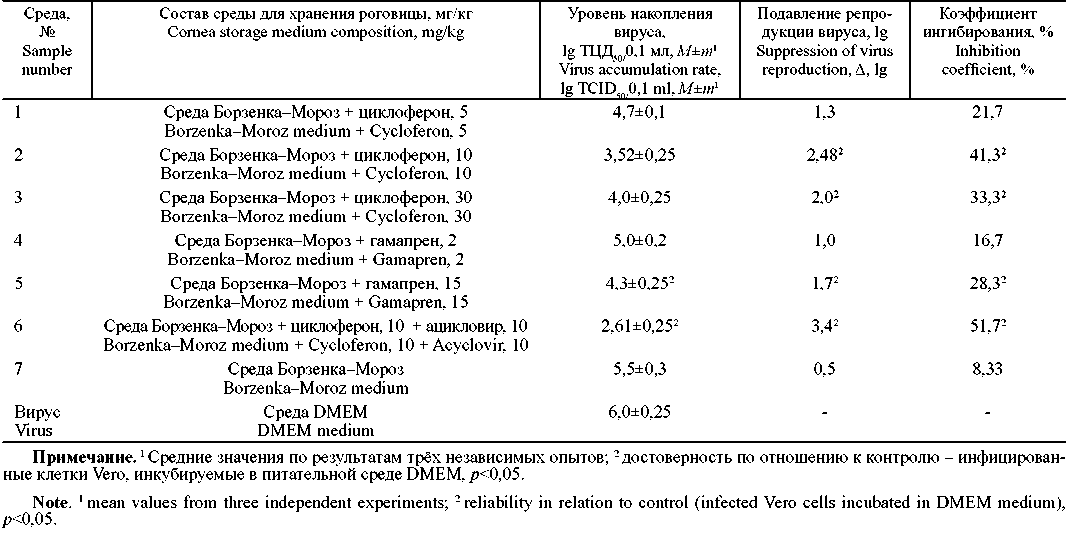
Results and discussion. All the studied images of the corneal storage medium, including the Borzenka-Moroz base medium, did not have a cytotoxic effect on Vero cell culture. Out of of 7 samples of liquid corneal storage medium, 4 samples had reliable antiviral activity against HSV-1 when used under the therapeutic regimen (1 hour after infection) and under the preventive regimen (2 hours before infection). Antiviral activity was established in 2 samples containing the interferon inducer cycloferon at a concentration of 10 mg/kg and 30 mg/kg (sample 2, 3), in a sample containing the interferon inducer gamapren 15 mg/kg (sample 5), and in a sample containing a combination of drugs - 10 mg/kg cycloferon and an acyclic nucleoside analog-acyclovir 10 mg/kg (sample 6). According to the results of 2 test regimens, the maximum statistically significant inhibitory effect in relation to HSV-1 was detected in sample 6, containing a combination of drugs. Against the background of sample 6, the infectious activity of the test virus decreased by an average of 3.2 lg, the inhibition coefficient was 54.5%.
Conclusion. The results of the study indicate the prospects of using types of media with antiviral activity (samples 2, 3, 5, 6) for storing donor corneas in order to increase the effectiveness of keratoplasty in patients with ophthalmic herpes.
 228-236
228-236