Prevalence of viral hepatitis B markers among blood donors in the Republic of Guinea
- Authors: Boumbaly S.1,2, Balde T.L.2, Semenov A.V.3, Ostankova Y.V.4, Serikova E.N.4, Naidenova E.V.5, Valutite D.E.4, Shchemelev A.N.4, Zueva E.B.4, Esaulenko E.V.4, Totolian A.A.4
-
Affiliations:
- International Tropical Infections Research Center
- Research Institute of Applied Biology of Guinea
- FSBI State Scientific Center of Virology and Biotechnology «Vector» of the Federal Service for Surveillance of Consumer Rights Protection and Human Wellbeing (Rospotrebnadzor)
- FBSI «Saint Petersburg Pasteur Research Institute of Epidemiology and Mictobiology» of the Federal Service for Surveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
- FSHI Russian Research Anti-Plague Institute «Microbe» of the Federal Service for Surveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
- Issue: Vol 67, No 1 (2022)
- Pages: 59-68
- Section: ORIGINAL RESEARCHES
- URL: https://journals.rcsi.science/0507-4088/article/view/118205
- DOI: https://doi.org/10.36233/0507-4088-92
- ID: 118205
Cite item
Abstract
Introduction. The problem of transfusion safety in relation to parenteral viral hepatitis still remains relevant. Viral hepatitis B (HB) remains the most common viral infection transmitted through transfusion procedures. One of the natural phases of chronic hepatitis B (CHB) is occult hepatitis B infection (OBI), characterized by an undetectable HBsAg (regardless of the other serological markers content) in the presence of hepatitis B virus (HBV) DNA in the liver tissue and an extremely low, up to undetectable, level of viral load in the blood. In the Republic of Guinea, as in most countries on the continent, the prevention of HBV transmission through transfusion is still based on HBsAg serological testing of donors only. In this connection, OBI remains as a potential threat to blood transfusion safety. Detection of HBV DNA is a reliable preventive measure against transmission of the virus from donors with HBsAg-negative HBV infection, especially in highly endemic regions. In this regard, the study was conducted to substantiate recommendations for improving blood safety against the background of significant HBV prevalence in the Republic of Guinea.
The aim of the work was the evaluation of serological and molecular markers of HBV infection in blood donors in the Republic of Guinea.
Material and methods. We examined 250 blood samples obtained from donors living in Conakry, Republic of Guinea. Samples were tested for the presence of serological (surface antigen, HBsAg; antibodies (ABs) to surface (anti-HBs IgG) and core (anti-HBc IgG) antigens) and molecular (DNA) markers of HBV infection.
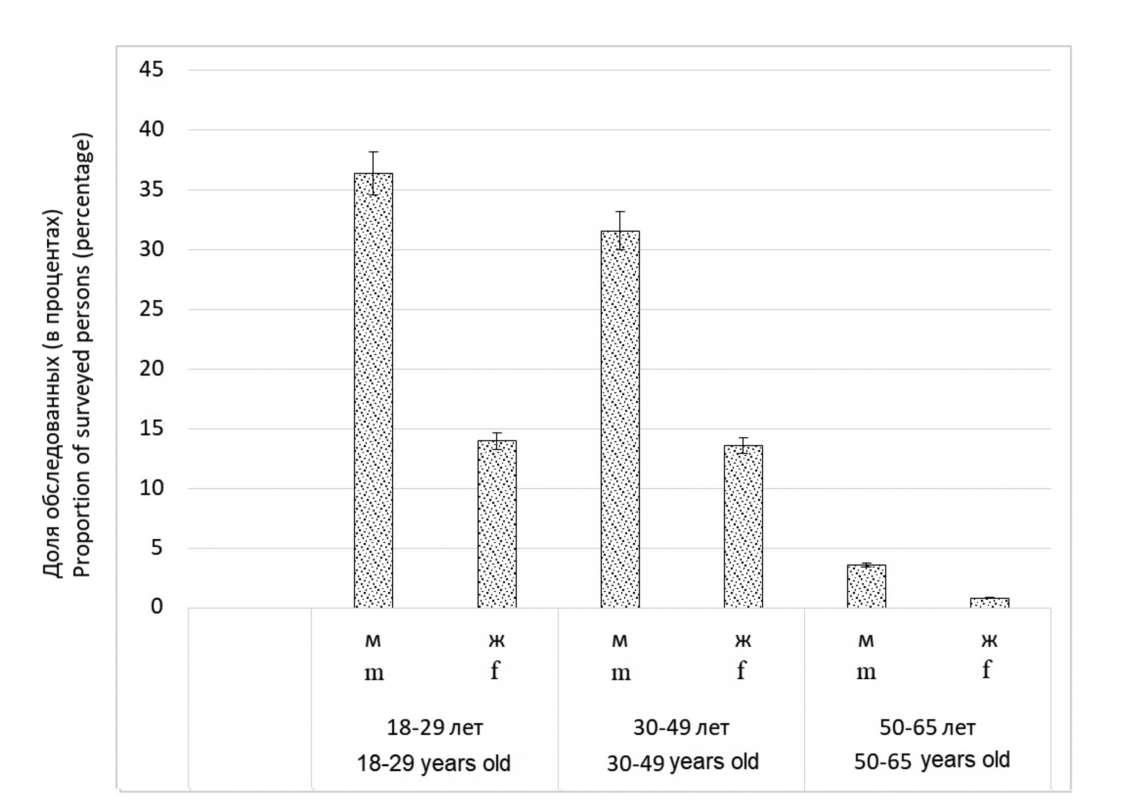
Results and discussion. The overall detection rate of hepatitis B markers was 83.2%; HBsAg was detected in 16.4% of all individuals. The high incidence of HBsAg in men (19.55%) compared to women (8.45%) was shown, the relative risk of HBV infection with the formation of HBsAg-positive chronic hepatitis B in males was also significantly higher. The prevalence of the HBV DNA in the study group was 30.4%, the OBI cases accounted for 15.6%. The prevalence of this form of the disease was shown in donors aged 30–49 years (24.78%), in the group of people younger than 30 years, the incidence was lower (8.73%), and at the age of over 50 years, OBI was not detected. Based on the phylogenetic analysis of 76 virus isolates, it was shown that genotype E prevails in the examined group (85.53%).
Cases of pathogen DNA detection occurred in HBsAg-negative blood donors in the presence of anti-HBs IgG (n = 4), as well as in the simultaneous presence of ABs anti-HBs IgG and anti-HBc IgG (n = 7). The viral load exceeded 200 IU/ml in OBI samples. Escape mutations were detected by sequencing in each OBI sample, contributing to the virus escaping from diagnostic based on screening for HBsAg.
Conclusion. Assessment of the prevalence viral hepatitis B markers in blood donors, determination of genotypes and clinically significant mutations of virus variants are necessary to ensure safe medical manipulations, control and prevention of the spread of this infectious agent.
Full Text
##article.viewOnOriginalSite##About the authors
S. Boumbaly
International Tropical Infections Research Center; Research Institute of Applied Biology of Guinea
ORCID iD: 0000-0002-4506-6033
Nzérékoré; Kindia
GuineaT.A. L. Balde
Research Institute of Applied Biology of Guinea
ORCID iD: 0000-0002-3808-4380
Kindia
GuineaA. V. Semenov
FSBI State Scientific Center of Virology and Biotechnology «Vector» of the Federal Service for Surveillance of Consumer Rights Protection and Human Wellbeing (Rospotrebnadzor)
ORCID iD: 0000-0003-3223-8219
630559, Novosibirsk Region, Kol’tsovo
Russian FederationYu. V. Ostankova
FBSI «Saint Petersburg Pasteur Research Institute of Epidemiology and Mictobiology» of the Federal Service forSurveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
Author for correspondence.
Email: shenna1@yandex.ru
ORCID iD: 0000-0003-2270-8897
Yulia V. Ostankova, Ph.D. (Biol.), Head of the HIV Infection Immunology and Virology Laboratory, Senior Researcher of the Molecular Immunology Laboratory
197101, Saint Petersburg
Russian FederationE. N. Serikova
FBSI «Saint Petersburg Pasteur Research Institute of Epidemiology and Mictobiology» of the Federal Service forSurveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
ORCID iD: 0000-0002-0547-3945
197101, Saint Petersburg
Russian FederationE. V. Naidenova
FSHI Russian Research Anti-Plague Institute «Microbe» of the Federal Service for Surveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
ORCID iD: 0000-0001-6474-3696
410005, Saratov
Russian FederationD. E. Valutite
FBSI «Saint Petersburg Pasteur Research Institute of Epidemiology and Mictobiology» of the Federal Service forSurveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
ORCID iD: 0000-0002-0931-102X
197101, Saint Petersburg
Russian FederationA. N. Shchemelev
FBSI «Saint Petersburg Pasteur Research Institute of Epidemiology and Mictobiology» of the Federal Service forSurveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
ORCID iD: 0000-0002-3139-3674
197101, Saint Petersburg
Russian FederationE. B. Zueva
FBSI «Saint Petersburg Pasteur Research Institute of Epidemiology and Mictobiology» of the Federal Service forSurveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
ORCID iD: 0000-0002-0579-110X
197101, Saint Petersburg
Russian FederationE. V. Esaulenko
FBSI «Saint Petersburg Pasteur Research Institute of Epidemiology and Mictobiology» of the Federal Service forSurveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
ORCID iD: 0000-0003-3669-1993
197101, Saint Petersburg
Russian FederationAreg A. Totolian
FBSI «Saint Petersburg Pasteur Research Institute of Epidemiology and Mictobiology» of the Federal Service forSurveillance of Consumer Rights Protection and Human Welfare (Rospotrebnadzor)
ORCID iD: 0000-0003-4571-8799
197101, Saint Petersburg
Russian FederationReferences
- Niederhauser C. Reducing the risk of hepatitis B virus transfusion-transmitted infection. J. Blood Med. 2011; 2: 91–102. https://doi.org/10.2147/JBM.S12899
- Candotti D., Assennato S.M., Laperche S., Allain J.P., Levicnik-Stezinar S. Multiple HBV transfusion transmissions from undetected occult infections: revising the minimal infectious dose. Gut. 2019; 68(2): 313–21. https://doi.org/10.1136/gutjnl-2018-316490
- Raimondo G., Locarnini S., Pollicino T., Levrero M., Zoulim F., Lok A.S., the Taormina Workshop on Occult HBV Infection Faculty Members. Update of the statements on biology and clinical impact of occult hepatitis B virus infection. J. Hepatol. 2019; 71(2): 397–408. https://doi.org/10.1016/j.jhep.2019.03.034
- Mulrooney-Cousins P.M., Michalak T.I. Persistent occult hepatitis B virus infection: experimental findings and clinical implications. World J. Gastroenterol. 2007; 13(43): 5682–6. https://doi.org/10.3748/wjg.v13.i43.5682
- Candotti D., Laperche S. Hepatitis B virus blood screening: need for reappraisal of blood safety measures? Front. Med. (Lausanne). 2018; 5: 29. https://doi.org/10.3389/fmed.2018.00029
- Серикова Е.Н., Семенов А.В., Останкова Ю.В., Тотолян Арег А. Метод выявления вируса гепатита В в плазме крови при низкой вирусной нагрузке с использованием ПЦР в режиме реального времени. Клини. Лаб. диагн. 2021; 66(1): 59–64. https://doi.org/10.18821/0869-2084-2021-66-1-59-64
- Эсауленко Е.В., Никитина О.Е., Порецкова Е.А., Писарева М.М. Вирусная нагрузка при хроническом гепатите В: корреляции с лабораторно-морфологическими показателями. Журнал инфектологии. 2012; 4(2): 67–72.
- Apica B.S., Seremba E., Rule J., Yuan H.J., Lee W.M. High prevalence of occult hepatitis B infection in an African urban population. J. Med. Virol. 2016; 88(4): 674–80. https://doi.org/10.1002/jmv.24372
- Loua A., Sow E.M., Magassouba F.B., Camara M., Baldé M.A. Evaluation of residual infectious risk among blood donors in National Center of Blood Transfusion in Conakry. Transfus. Clin. Biol. 2004; 11(2): 98–100. https://doi.org/10.1016/j.tracli.2004.01.004 (in French)
- Delamou A., Haba N.Y., Mari-Saez A., Gallian P., Ronse M., Jacobs J., et al. Organizing the donation of convalescent plasma for a therapeutic clinical trial on Ebola virus disease: the experience in Guinea. Am. J. Trop. Med. Hyg. 2016; 95(3): 647–53. https://doi.org/10.4269/ajtmh.15-0890
- Найденова Е.В., Лопатин А.А., Сафронов В.А., Коломоец Е.В., Левковский А.Е., Силла А.Л., и др. Обеспечение биологической безопасности при проведении противоэпидемических мероприятий в период ликвидации эпидемии лихорадки Эбола в Гвинейской Республике. Инфекционные болезни: новости, мнения, обучение. 2018; 7(3): 102–8. https://doi.org/10.24411/2305-3496-2018-13015
- Brichler S., Lagathu G., Chekaraou M.A., Le Gal F., Edouard A., Dény P., et al. African, Amerindian and European hepatitis B virus strains circulate on the Caribbean Island of Martinique. J. Gen. Virol. 2013; 94(Pt. 10): 2318–29. https://doi.org/10.1099/vir.0.055459-0
- Hønge B.L., Olesen J.S., Jensen M.M., Jespersen S., da Silva Z.J., Rodrigues A., et al. Hepatitis B and C in the adult population of Bissau, Guinea-Bissau: a cross-sectional survey. Trop. Med. Int. Health. 2020; 25(2): 255–63. https://doi.org/10.1111/tmi.13335
- Osaro E., Charles A.T. The challenges of meeting the blood transfusion requirements in Sub-Saharan Africa: the need for the development of alternatives to allogenic blood. J. Blood Med. 2011; 2: 7–21. https://doi.org/10.2147/JBM.S17194
- Allain J.P., Candotti D., Soldan K., Sarkodie F., Phelps B., Giachetti C., et al. The risk of hepatitis B virus infection by transfusion in Kumasi, Ghana. Blood. 2003; 101(6): 2419–25. https://doi.org/10.1182/blood-2002-04-1084
- Bes M., Vargas V., Piron M., Casamitjana N., Esteban J.I., Vilanova N., et al. T cell responses and viral variability in blood donation candidates with occult hepatitis B infection. J. Hepatol. 2012; 56(4): 765–74. https://doi.org/10.1016/j.jhep.2011.11.011
- Zerbini A., Pilli M., Boni C., Fisicaro P., Penna A., Di Vincenzo P., et al. The characteristics of the cell-mediated immune response identify different profiles of occult hepatitis B virus infection. Gastroenterology. 2008; 134(5): 1470–81. https://doi.org/10.1053/j.gastro.2008.02.017
- Makvandi M. Update on occult hepatitis B virus infection. World J. Gastroenterol. 2016; 22(39): 8720–34. https://doi.org/10.3748/wjg.v22.i39.8720
- Щемелев А.Н., Останкова Ю.В., Зуева Е.Б., Boumbaly S., Balde T.A.L., Семенов А.В. Характеристика вируса гепатита B и вируса иммунодефицита человека среди пациентов с коинфекцией ВИЧ/ВГВ из Гвинейской Республики. Проблемы особо опасных инфекций. 2019; (3): 118–24. https://doi.org/10.21055/0370-1069-2019-3-118-124
- Балде T.A.Л., Бумбали С., Серикова Е.Н., Валутите Д.Э., Щемелев А.Н., Останкова Ю.В., и др. Сравнительный анализ вертикального риска передачи некоторых гемоконтактных инфекций в Гвинейской Республике. Проблемы особо опасных инфекций. 2021; (1): 87–94. https://doi.org/10.21055/0370-1069-2021-1-87-94
- Diarra B., Yonli A.T., Sorgho P.A., Compaore T.R., Ouattara A.K., Zongo W.A., et al. Occult hepatitis B virus infection and associatedgenotypes among HBsAg-negative subjects in Burkina Faso. Mediterr. J. Hematol. Infect. Dis. 2018; 10(1): e2018007. https://doi.org/10.4084/MJHID.2018.007
- Allain J.P., Candotti D. Diagnostic algorithm for HBV safe transfusion. Blood Transfus. 2009; 7(3): 174–82. https://doi.org/10.2450/2008.0062-08
- Garmiri P., Loua A., Haba N., Candotti D., Allain J.P. Deletions and recombinations in the core region of hepatitis B virus genotype E strains from asymptomatic blood donors in Guinea, west Africa. J. Gen. Virol. 2009; 90(Pt. 10): 2442–51. https://doi.org/10.1099/vir.0.012013-0
- Ostankova Yu.V., Semenov A.V., Zueva E.B., Totolian Areg A. The first cases of Hepatitis B virus subgenotype D4 detection in patients with chronic, acute, and occult hepatitis B in the Russian Federation. Mol. Gen. Microbiol. Virol. 2020; 35: 221–8. https://doi.org/10.3103/S0891416820040072
Supplementary files