Neuroimaging of full term newborn´s brain with hypoxic-ischemic encephalopathy
- Authors: Melashenko T.V1, Pozdnyakov A.V1, Alexandrov T.A1
-
Affiliations:
- St Petersburg State Pediatric Medical University
- Issue: Vol 7, No 3 (2016)
- Pages: 157-161
- Section: Articles
- URL: https://journals.rcsi.science/pediatr/article/view/5738
- DOI: https://doi.org/10.17816/PED73157-161
- ID: 5738
Cite item
Full Text
Abstract
Keywords
Full Text
Актуальность
Гипоксически-ишемическая энцефалопатия (ГИЭ) рассматривается как одна из основных причин смертности в перинатальном периоде и развития неврологических нарушений у новорожденных детей [9]. Частота ГИЭ у доношенных новорожденных составляет 1,8–6,0 % на 1000 живорожденных [11]. Неврологические нарушения выявляются у 25 % выживших доношенных новорожденных, перенесших ГИЭ тяжелой степени [7]. Тяжелые неврологические осложнения развиваются в отдаленном периоде у 90 % детей, у которых в первые две недели жизни выявлены постгипоксические структурные изменения методом магнитно-резонансной томографии (МРТ) [1, 5, 6, 10]. Отмечается корреляция МР-изменений головного мозга и неврологических нарушений у детей, перенесших ГИЭ [16]. Основными МРТ-паттернами ГИЭ у доношенных новорожденных являются повреждения базальных ганглиев и ядер зрительного бугра [3, 8].
Методы исследования
Представлены результаты клинико-инструментального обследования двух доношенных новорожденных, перенесших интранатальную асфиксию тяжелой степени с клиникой ГИЭ (пациент С. и пациент М.). Диагноз ГИЭ установлен в соответствии с критериями, определенными Американской педиатрической академией [17]. Тяжесть ГИЭ у данных новорожденных детей, определяемая по классификации ГИЭ, предложенная Sarnat & Sarnat, соответствовала третьей степени [15].
Скрининговая КС выполнялась на 1, 3, 5 и 14-е сутки жизни по общепринятой методике с использованием микроконвексного (5 МГц) и линейного датчиков (7,5 МГц) (аппарат Philips HD10XE). МРТ головного мозга (томограф Philips Ingenia 1,5 Tl) проводилась на 14–16-й день жизни. Использовались стандартные протоколы исследования головного мозга у новорожденных детей и DTI. Значения КФА определялись в зоне прохождения кортикоспинального тракта (КСТ) в области задней ножки внутренней капсулы на уровне нижних отделов зрительных бугров с обеих сторон КСТ. МРТ выполнялась без седации пациентов с мониторированием витальных функций. Пациенту (С.) выполнена повторная МРТ головного мозга (на 6-й неделе жизни). Дополнительно проведена однократная МРТ головного мозга доношенным новорожденным без клинико-инструментальных признаков повреждения головного мозга в возрасте 15–16 суток (группа контроля).
Результаты
Пациент C. Ребенок от первой физиологической беременности, срочные самостоятельные роды, длительность безводного периода 10 часов, развитие вторичной слабости родовой деятельности, потребовавшее проведения вакуум-экстракции головки плода. Состояние крайне тяжелое, оценка по шкале Апгар составила 1/3/4 балла. Инвазивная респираторная терапия начата в первые 30 минут жизни. Манифестация ГИЭ отмечалась с первых суток жизни угнетением сознания (кома 1), выраженной мышечной гипотонией, арефлексией, кратковременными (до 20 с) эпизодами полифокальных клонических судорог со вторых суток жизни. Длительность угнетения сознания составила 7 суток. С пятых суток отмечались трансформация патологического мышечного тонуса (появилась асимметричная мышечная гипертония по экстрапирамидному типу), приступы гиперкинезов в виде кратковременных патологических установок головы, сопровождающиеся гипертонусом сгибателей конечностей, низкоамплитудным генерализованным тремором, периодическими движениями нижних конечностей по типу педалирования. С первых суток определялась симметричная оживленность глубоких рефлексов.
При краниальной сонографии выявлены постгипоксические изменения: симметричное усиление эхосигнала от базальных ядер и зрительных бугров с первых суток жизни (рис. 1).
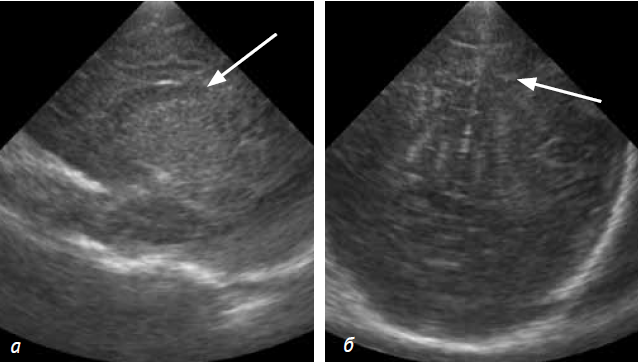
Рис. 1. Пациент C. Краниальная сонография (первые сутки жизни), парасагиттальный (а) и фронтальный (б) срезы. Стрелками отмечены участки усиления эхосигналов от зрительного бугра и базальных ядер
МР-изменения (на 16-е сутки жизни) включали патологическое усиление МР-сигнала на Т1 ВИ и Flair от бледного шара, вентролатеральных ядер зрительных бугров, лентиформных ядер с обеих сторон (рис. 2). Усиление МР-сигнала на Т1 ВИ отмечалось также от гиппокампальной и парагиппокампальной извилин, по ходу КСТ. Значения КФА в симметричных зонах прохождения кортикоспинального тракта представлены в таблице № 1. Контрольная МРТ головного мозга выполнена в возрасте 6 недель. Сохраняется усиление МР-сигнала на Т1 ВИ и Flair ВИ от бледного шара и вентролатеральных ядер зрительных бугров, лентиформных ядер, гиппокампальной и парагиппокампальной извилин, по ходу кортикоспинального тракта. С обеих сторон на фоне вышеописанных изменений прослеживаются сформировавшиеся ликворные кисты, расположенные у наружного края передних отделов внутренней капсулы (рис. 3).
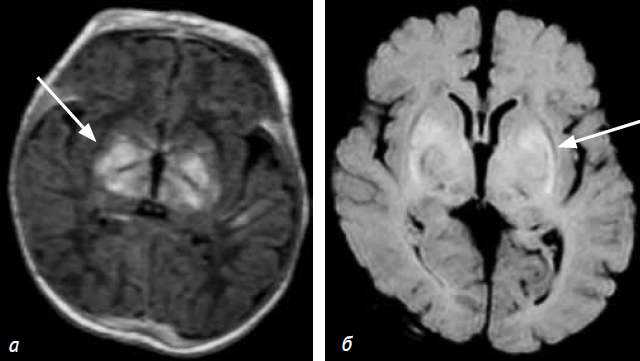
Рис. 2. Пациент C. (16 дней), Т1 ВИ (а, б) и Flair (б). Определяются патологические гиперинтенсивные МР-сигналы от вентролатеральных ядер зрительных бугров (а), бледного шара (б)
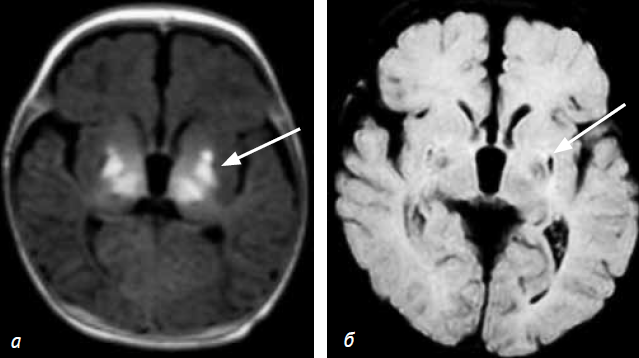
Рис. 3. Пациент C. МРТ головного мозга в возрасте 6 недель (контрольная группа): Т1 ВИ (а) и Flair (б). Определяются гиперинтенсивные МР-сигналы от вентролатеральных ядер зрительного бугра и лентиформных ядер (а). Прослеживаются сформировавшиеся кисты, расположенные в области скорлупы с обеих сторон (б)
Пациент М. Доношенный мальчик от физиологически протекавшей беременности, вторые срочные оперативные роды (отслойка нормально расположенной плаценты), оценка по шкале Апгар 1/3/4 балла, проведение искусственной вентиляции легких (ИВЛ) в родильном зале. Развитие судорог (повторные генерализованные тонические приступы) отмечалось в первые сутки жизни, угнетение сознания с первых суток (кома 2). Поступил на отделение на 2-е сутки жизни в крайне тяжелом состоянии. Продолжительность ИВЛ составила 5 суток, угнетение сознания отмечалось до 8 суток жизни. Определялась очаговая неврологическая симптоматика: диффузная мышечная гипотония, патологическое усиление глубоких рефлексов, сходящийся паралитический страбизм.
Краниальная сонография, выполненная в день поступления и в динамике, выявила симметричное изменение эхосигнала в области зрительных бугров.
Результаты МРТ головного мозга (14-й день жизни): в области бледного шара с обеих сторон, в области скорлупы, в зонах таламусов с обеих сторон визуализируются участки повышения МР-сигнала на Т1 ВИ, Flair (рис. 4). На 3D-изображениях, полученных в результате постпроцессинговой обработки с помощью программы Fiber tracking, визуализируются участки кортикоспинальных трактов с обеих сторон, ход и направление их не изменены (рис. 5). Также отмечались повышения МР-сигнала на DWI от зрительных бугров. МРТ головного мозга у новорожденных детей контрольной группы, выполненная на 14-й день жизни, патологических изменений в головном мозге не выявила. Сравнительный анализ результатов КФА КСТ у новорожденных детей с ГИЭ и контрольной группы выявил снижение значений КФА в зоне интереса (ROI) и общего КФА КСТ при повреждении базальных ганглиев и зрительных бугров (см. табл. 1).
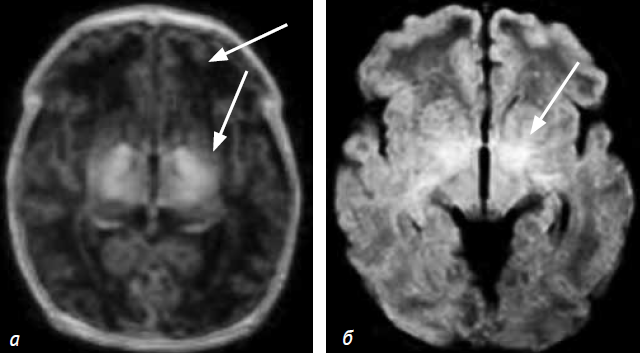
Рис. 4. Пациент М. МРТ головного мозга выполнена на 14-й день жизни: Т1 ВИ (а) и Flair (б). Визуализируются участки патологического усиления МР-сигнала на Т1 ВИ и Flair в области бледного шара и в зрительных буграх с обеих сторон
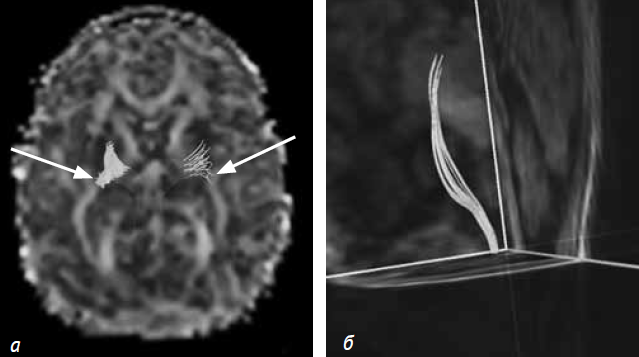
Рис. 5. Пациент М. (16-й день жизни). 3D-визуализация. Визуализируются участки кортикоспинального тракта без макроизменений (а); б — участок левостороннего кортикоспинального тракта
Таблица 1. Значения коэффициента фракционной анизотропии в местах прохождения кортикоспинального тракта у обследованных детей (доношенных новорожденных с гипоксически-ишемической энцефалопатией и доношенных новорожденных группы контроля)
Зоны определения КФА | Значения КФА пациентов с гипоксически-ишемической энцефалопатией | Значения КФА новорожденных контрольной группы | ||||||
Пациент С. | Пациент М. | Новорожденный № 1 | Новорожденный № 2 | |||||
КФА | девиация КФА | КФА | девиация КФА | КФА | девиация КФА | КФА | девиация КФА | |
Общий КФА справа | 0,256 | ± 0,082 | 0,242 | ± 0,087 | 0,296 | ± 0,105 | 0,300 | ± 0,127 |
Общий КФА слева | 0,262 | ± 0,088 | 0,231 | ± 0,067 | 0,282 | ± 0,011 | 0,340 | ± 0,110 |
ROI справа | 0,269 | ± 0,079 | 0,254 | ± 0,097 | 0,280 | ± 0,109 | 0,347 | ± 0,127 |
ROI слева | 0,264 | ± 0,054 | 0,251 | ± 0,081 | 0,298 | ± 0,143 | 0,295 | ± 0,126 |
КФА — коэффициент фракционной анизотропии; ROI — зона интереса определения КФА на уровне задней ножки внутренней капсулы в проекции нижних отделов зрительных бугров | ||||||||
Обсуждение
Результаты обследования представленных пациентов выявили клинические и нейровизуализационные паттерны повреждения головного мозга, характерные для ГИЭ у доношенных новорожденных, что было отмечено и другими исследователями [14]. Основной нейровизуализационный паттерн постгипоксических изменений головного мозга представлен повреждением зрительных бугров и базальных ганглиев. Это связано с тем, что эти области имеют высокую метаболическую активность и часто повреждаются [3]. Подобные изменения характеризуются усилением (пациенты С. и М.) эхосигнала от базальных ганглиев и зрительных бугров в остром периоде ГИЭ, что подтверждается данными МРТ. Характерные МРТ-паттерны ГИЭ у доношенных новорожденных диагностированы на 14–16-й день жизни, которые характеризовались изменением сигнала в течение 6 недель (контрольная МРТ пациента С.). При этом были выявлены изменения в гиппокампах (пациент С.). Полученные данные также были подтверждены другими исследователями [4, 10, 12]. Следует отметить, что у пациентов изменения выявлялись в зонах, прилегающих к КСТ, в виде усиления сигнала от перивентрикулярных зон (пациент М.) и наличия ликворных кист у переднего отдела внутренней капсулы (пациент С.) без признаков повреждения тракта. Предполагается возможность изменений микроструктуры проводящих путей (и прежде всего КСТ) в случаях повреждения базальных ганглиев и зрительных бугров у доношенных новорожденных с ГИЭ [2, 18]. В нашем исследовании (см. табл. 1) выявленное изменение КФА КСТ при повреждении базальных ганглиев и зрительных бугров может служить подтверждением предположения о нарушении микроструктур проводящих трактов у новорожденных детей с ГИЭ. Вторая возможная причина изменения КФА КСТ у новорожденных детей с постгипоксическим повреждением зрительных бугров и базальных ганглиев может быть связана с нарушением/задержкой миелинизации трактов у таких новорожденных, что нашло подтверждение в работах других исследователей [19]. Однако интерпретация данных трактограмм, результатов данных фракционной анизотропии осложняется отсутствием «норм» для новорожденных различного гестационного возраста. Трактография в настоящее время представляет предмет научных исследований головного мозга новорожденных детей и является наиболее перспективным методом изучения проводящих путей in vivo [13].
Таким образом, основными МР-паттернами ГИЭ у доношенных новорожденных являются повреждения базальных ганглиев и зрительных бугров, а дополнительными — изменения гиппокампа и зон, прилегающих к КСТ. Патологическая гиперинтенсивность МР-сигналов от зрительных бугров и базальных ганглиев может сохраняться в течение 6 недель после перенесенной асфиксии. Использование режима DTI при проведении МРТ головного мозга у доношенных новорожденных с ГИЭ и повреждением базальных ганглиев и зрительных бугров выявляет снижение общего значения КФА с обеих сторон КСТ и снижение КФА КСТ в области задней ножки внутренней капсулы. Применение DTI может использоваться как исследование, дополняющее стандартные методы МРТ головного мозга у новорожденных детей с ГИЭ.
About the authors
Tatiana V Melashenko
St Petersburg State Pediatric Medical University
Author for correspondence.
Email: melashenkotat@mail.ru
MD, PhD. Anesthesiology and Intensive Care Neonatal Perinatal Center Russian Federation
Alexander V Pozdnyakov
St Petersburg State Pediatric Medical University
Email: pozdnyakovalex@ya.ru
MD, PhD, Dr Med Sci, Professor, Head. Department of Medical Biophysics, Radiology Department Russian Federation
Timofey A Alexandrov
St Petersburg State Pediatric Medical University
Email: ale-tim@list.ru
Department of Medical Biophysics, Radiology Department Russian Federation
References
- Мелашенко Т.В., Гузева В.В. Особенности транзиторной биоэлектрической активности головного мозга у недоношенных детей с перинатальным гипоксически-ишемическим поражением центральной нервной системы // Педиатр. — 2014. — Т. 5. — № 1. — С. 32–36. [Melashenko TV, Guzeva VV. Particular transit patterns EEG in premature babies with hypoxia-ischemic encephalopathy. Pediatr (St Petersburg). 2014;5(1):32-36. (In Russ).]
- Aeby A, Liu Y, Tiege X De, et al. Maturation of Thalamic Rediations between 34 and 41 Weeks Gestation: A Combined Voxel — Based Study and Probabilitic tractography with Diffusion Tensor Imaging. AJNR. 2009;30:1780-1786. doi: 10.3174/ajnr.A1660.
- Ball C, Boardman James P, Daniel Rueckert, et al. The Effect of Preterm Birth on Thalamic and Cortical Development. Cerebral Cortex. 2012;22(5):1016-1024. doi: 10.1093/cercor/bhr176.
- Barkovich AJ, Westmark K, Partridge C, et al. Perinatal asphyxia: MR findings in the first ten days. JNR. 1995;16:427-438.
- Cabaj AG, Bekiesin’ska-Figatowska M., Madzic J. MRI patterns of hypoxic — ischemic brain injury in preterm and full term infants — classical and less common MR findings. Pol J Radiol. 2012;77(3):71-76. doi: 10.12659/PJR.883379.
- Cowan F, Rutherford M, Groenendaal F, et al. Origin and timing of brain lesions in term infants with neonatal encephalopathy. Lancet. 2003;361:736-742. doi: 10.1016/S0140-6736(03)12658-X.
- Dergans M, Osredkar D. Hypoxic-ischemic brain injury in the neonatal period — current concepts, novel diagnostic approaches and neuroprotective strategies. Zdrav Vestn. 2008;77(II):51-8.
- Himmelmann K, Hagberg G, Wiklund LM, et al. Dyskinetic cerebral palsy: a population-based study of children born between 1991 and 1998. Dev Med Child Neurol. 2007;49:246-251. doi: 10.1111/j.1469-8749.2007.00246.x.
- Kurinczuk JJ, White-Koning M, Badawi N. Epidemiology of neonatal encephalopathy and hypoxic-ischaemic encephalopathy. Early Hum Dev. 2010;86:329-338. doi: 10.1016/j.earlhumdev.2010.05.010.
- Linda S. de Vries, Groenendaal F. Patterns of neonatal hypoxic-ischaemic brain injury. Neuroradiology. 2010;52:555-566.
- Linda S de Vrries, Jongmans MJ. Long-term outcome after neonatal hypoxic — ischaemic encephalopathy. Arch Dis Child Fetal Neonatal Ed. 2010;95: F220-F224. doi: 10.1007/s00234-010-0674-9.
- Nikas I, Dermentzoglou V, Theotanopoulou M, Theodoropoulos V. Parasagittal Lesions and Ulegyria in Hypoxic-Ischemic Encephalopathy: Neuroimaging Findings and Review of the Pathogenesis. Child Neurol. 2008;23(1):51-58. doi: 10.1177/0883073807308694.
- Nucitora PGP, Verma R, Lee S-K, Methem ER. Diffusion — Tensor MR Imaging and Tractography: Exploring Brain Microstructure and Connectivity. Radiology. 2007;245:367-384. doi: 10.1148/radiol.2452060445.
- Rosenbloom L. Dyskinetic cerebral palsy and birth asphyxia. Dev Med Child Neurol. 1994;36(4):285-289. doi: 10.1111/j.1469-8749.1994.tb11848.x.
- Sarnat HB, Sarnat MS. Neonatal encephalopathy following fetal distress: a clinical and electroencephalographic study. Archives of Neurology. 1976;33:696-705. doi: 10.1001/archneur.1976.
- Ten Vadim S, Tang Haijing, Bradley-Moore M, et al. Late Measures of Brain Injury After Neonatal Hypoxia-Ischemia in Mice. Stroke. 2004;35:2183-2188. doi: 10.1161/01.STR.0000137768.25203.df.
- Twomey E, Twomey A, Ryan S, et al. MR imaging of term infants with hypoxic — ischaemic encephalopathy as a predictor of neurodevelopmental outcome and late MRI appearance. Pediatr Radiol. 2010;40:1526-1535. doi: 10.1007/s00247-010-1692-9.
- Volpe JJ. Brain injury in premature infants: a complex amalgam of destructive and developmental disturbances. Lancet Neurol. 2009;8:110-124. doi: 10.1016/S1474-4422(08)70294-1.
- Yeatman JD, MB-Shachar, Bammer R, Feldman HM. Using Diffusion Tensor Imaging and Fiber Tracing to Characterize Diffuse perinatal White Matter Injury: A case Report. J of Child Neurology. 2009;24:794-800. doi: 10.1177/0883073808331080.
Supplementary files







