Case of heart disease in mixed streptococcal and Epstein - Barr virus infection
- Authors: Levina A.S1, Babachenko I.V1, Chuprova S.N2, Kochevaya N.V2, Sharipova E.V2, Ibragimova O.M2
-
Affiliations:
- St Petersburg State Pediatric Medical University
- Federal Medico-Biological Agency of Russia
- Issue: Vol 7, No 3 (2016)
- Pages: 147-152
- Section: Articles
- URL: https://journals.rcsi.science/pediatr/article/view/5736
- DOI: https://doi.org/10.17816/PED73147-152
- ID: 5736
Cite item
Full Text
Abstract
Full Text
Клинический случай
Хорошо известна связь многочисленной кардиологической патологии с инфекционными заболеваниями вирусной и бактериальной этиологии. При инфекционных заболеваниях могут поражаться все оболочки сердца, однако чаще страдает миокард. Миокардит при инфекционных заболеваниях у взрослых развивается в 5–20 % [3, 7]. Частота миокардитов у детей неизвестна в связи с отсутствием единых диагностических критериев, чрезвычайного разнообразия клинической симптоматики заболевания (от малосимптомных, «стертых» форм до тяжелых), а также почти полным отсутствием координируемых многоцентровых исследований [1].
В настоящее время под термином «миокардит» понимают воспалительные заболевания сердечной мышцы, вызываемые прямым действием инфекционного агента или опосредованным его действием через механизм предварительной аллергизации или аутоиммунизации [8].
Вирусы являются наиболее частым этиологическим фактором миокардитов, вызывая до 80 % случаев заболевания в индустриальных странах мира [9]. Чаще всего воспаление миокарда выявляется как осложнение острых респираторных вирусных инфекций, поэтому заболеваемость увеличивается во время эпидемических вспышек. По данным ВОЗ, установлено, что при заражении вирусами Коксаки группы А воспалительное поражение сердечной мышцы развивается в 2,9 % случаев, при гриппе А — в 1,4 %, при гриппе В — в 1,2 %, при парагриппе — в 1,7 %, при аденовирусных инфекциях — 1,0 %, при воздействии вирусов герпеса — в 0,4 % случаев [5]. Однако в некоторых исследованиях показана высокая частота миокардитов при Эпштейна — Барр вирусном инфекционном мононуклеозе (в 8 % случаев) [6].
После бактериальных инфекций воспаление мышцы сердца развивается в 4–5 % случаев. Среди микробных возбудителей наибольшее значение в этиологии миокардитов принадлежит стрептококкам группы А, возбудителям дифтерии, брюшного тифа, стафилококкам, менингококкам, пневмококкам [5].
В кардиологических стационарах пациенты с диагнозом «миокардит» составляют не более 1 % от общего числа больных, но считается, что это не отражает истинной распространенности заболевания [7]. Неучтенными остаются и многие случаи миокардита при вирусных и бактериальных заболеваниях [4].
Трудности выявления кардиальных поражений обусловлены вариабельностью клинической картины миокардитов, которая зависит от степени распространенности и локализации изменений в миокарде. При диффузном поражении сердечной мышцы развиваются признаки сердечной недостаточности; ограниченный воспалительный процесс, локализованный в области проводящей системы сердца, может привести как к незначительным (АВ-блокада I степени), так и к серьезным последствиям (АВ-блокады, желудочковые аритмии высоких градаций) [2]. Сердцебиения (тахикардия) весьма характерны для миокардита и связаны с активацией симпато-адреналовой системы, развивающейся на фоне уменьшения ударного выброса [2]. Кардиальная симптоматика может практически отсутствовать при легких и субклинических формах. В терапевтической практике для диагностики миокардита используются критерии NYHA (1973), рекомендованные Нью-Йоркской ассоциацией кардиологов.
Диагноз миокардита наиболее обоснован, если после перенесенной инфекции в течение 10 дней (по некоторым данным — 2–3 недель) выявляются большие (застойная сердечная недостаточность, кардиогенный шок, полная AВ-блокада, патологические изменения электрокардиограммы (ЭКГ), повышение активности миокардиальных энзимов) и малые (лабораторное подтверждение перенесенного вирусного заболевания, тахикардия, ослабление І тона, ритм галопа, результаты субэндомиокардиальной биопсии) диагностические критерии. Данные анамнеза и сочетание двух больших или одного большого и двух малых критериев достаточны для установления диагноза [2]. «Золотым стандартом» диагностики миокардита является метод эндомиокардиальной биопсии (ЭМБ). Однако риски развития осложнений при выполнении этой процедуры достигают 6 %, частота возникновения перфорации миокарда составляет 0,5 %. Различия в интерпретации биоптатов оказывают существенное негативное влияние на полученные результаты. Показания к проведению ЭМБ в соответствии с рекомендациями Американской ассоциации кардиологов ограничены быстропрогрессирующей кардиомиопатией, рефрактерной к стандартному лечению, и кардиомиопатией с прогрессирующим поражением проводящей системы [7].
В случаях малосимптомного или бессимптомного вариантов острого миокардита нередко единственным симптомом, указывающим на возможное наличие воспалительного поражения миокарда, является отрицательная динамика ЭКГ (смещение сегмента S-Т, изменения зубца Т или появление нарушений АВ-проводимости) [2].
Мы представляем описание клинического случая вирусно-бактериальной инфекции, осложненной развитием острого миокардита, у девочки 11 лет.
Ребенок поступил 4 апреля на 6-й день болезни с жалобами на недомогание, повышение температуры до 38 °C, увеличение и болезненность шейных лимфоузлов, заложенность носа, храпящее дыхание ночью.
Анамнез болезни. С октября отмечались повторные эпизоды ринофарингита, ангина, заложенность носа, периодически сильный кашель, изредка повышение температуры. За этот период девочка получила 4 курса антибиотиков (три 5-дневных курса препаратов пенициллинового ряда, один 10-дневный курс цефалоспорина 2-го поколения) с кратковременным эффектом. С 30 марта отмечали увеличение лимфоузлов справа, заложенность носа. С 3 апреля регистрировали повышение температуры до 38 °C, резкую болезненность шейных лимфоузлов справа.
Амбулаторно было проведено серологическое исследование крови на антитела к вирусу Эпштейна – Барр (ВЭБ) методом иммуноферментного анализа (ИФА), по результатам которого выявлены антитела класса IgG к капсидному антигену вируса (VCA) при отсутствии IgM к VCA.
4 апреля родители самостоятельно обратились в детскую городскую больницу, где ребенок был осмотрен хирургом и ЛОР-врачом. Диагностирован острый ринофарингит, заподозрен инфекционный мононуклеоз. В гемограмме выявлен лейкоцитоз 12,8 × 109/л за счет нейтрофилеза (87 %) с незначительным сдвигом формулы влево до 5 % палочкоядерных форм, СОЭ повышена до 20 мм/ч, токсическая зернистость нейтрофилов ++. Для дальнейшего обследования и лечения ребенок переведен в клинику ФГБУ НИИДИ ФМБА России.
Из анамнеза жизни известно, что ребенок от первой нормально протекавшей беременности, срочных родов, масса тела при рождении 3570 г, искусственное вскармливание на первом году жизни, привита по возрасту, аллергологический анамнез без особенностей. Материально-бытовые условия благоприятные. Частые респираторные заболевания отмечают с 3 лет. Наблюдалась ЛОР-врачом по поводу рецидивирующего синусита.
При поступлении состояние средней тяжести, контактна, активна, неплохой аппетит, кожные покровы обычной окраски, без сыпи, склеры обычной окраски; в зеве разлитая, умеренно выраженная гиперемия, слизистые ротовой полости чистые; миндалины гипертрофированы I степени без налетов. Справа передне- и заднешейные лимфоузлы до 3 см в диаметре в виде пакетов, плотноэластичные, болезненные при пальпации и поворотах головы, слева — до 1,5–2 см, плотноэластичные, безболезненные. Отека в зеве и подкожной клетчатки шеи нет. При аускультации легких дыхание везикулярное 22 в минуту, хрипы не выслушиваются. Границы сердца не расширены. Тоны сердца ритмичные, звучные, 68 ударов в минуту. Язык обложен белым налетом. Живот при поверхностной пальпации мягкий, безболезненный; печень не увеличена; селезенка не увеличена. Стул оформлен, 1 раз в день. Диурез сохранен.
При обследовании методом полимеразной цепной реакции (ПЦР) выявлена ДНК вируса Эпштейна — Барр в крови в диагностическом количестве и повышенный до 880 Ед уровень антистрептолизина-О (АСЛ-О), на основании чего диагностирована смешанная вирусно-бактериальная инфекция: инфекционный мононуклеоз ВЭБ этиологии средней степени тяжести на фоне хронической стрептококковой инфекции.
Уровень аланинаминотрансферазы (АлТ) и С-реактивного белка (СРБ) в норме. Общий анализ мочи, копрограмма без признаков патологии. В посеве отделяемого из рото- и носоглотки патогенных и условно-патогенных микроорганизмов не обнаружено. ПЦР крови на ДНК цитомегаловируса и вируса герпеса человека 6-го типа отрицательная. При иммуноцитохимическом исследовании мазков со слизистой задней стенки глотки антигенов хламидий (C. trachomatis) и микоплазм (M. pneumoniae) не обнаружено.
На ЭКГ от 9 апреля (11-й день болезни) отмечена синусовая тахикардия и единичные экстрасистолы.
С поступления начата терапия цефтриаксоном 50 мг/кг в сутки, местная терапия фарингита, с 9 апреля — противовирусная терапия препаратом рекомбинантного интерферона-α по 500 тыс. МЕ 2 раза в день.
В ходе лечения к 6 апреля (8-й день болезни) состояние улучшилось — нормализовалось самочувствие, аппетит, температура. К 9 апреля шейные лимфатические узлы уменьшились до 2 см, слабочувствительные при пальпации.
С 9 апреля (11-й день болезни) периодически отмечались подъемы температуры до субфебрильных цифр. В клиническом анализе крови лейкоцитоз до 13,7 × 109/л за счет нейтрофилеза, отмечено увеличение СОЭ до 33 мм/ч. Общий анализ мочи без патологии. Динамика лабораторных показателей представлена на рисунке 1.
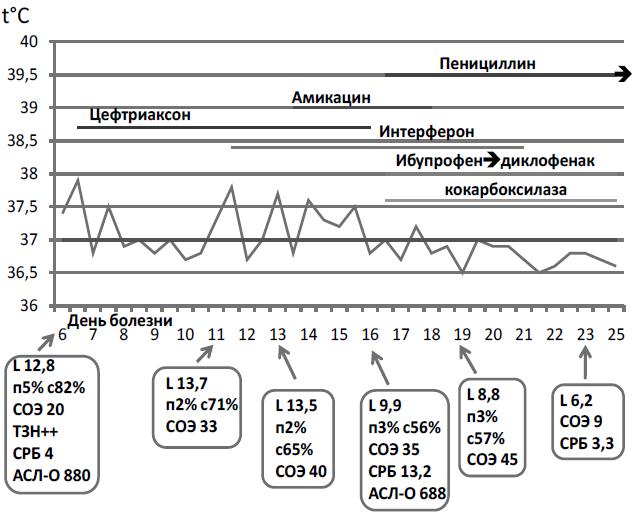
Рис. 1. Температурный лист пациента
11 апреля (13-й день болезни) утром пациентка пожаловалась на головную боль, резкую слабость. При осмотре кожные покровы обычной окраски, зев гиперемирован умеренно, налетов нет, периферические лимфоузлы не увеличены, безболезненны, эластичны, до 1,3 см. Частота дыхания 22 в минуту, везикулярное дыхание в легких. При аускультации сердца отмечена тахикардия: ЧСС лежа 104 удара в минуту, стоя — 128 ударов в минуту; тоны сердца ритмичные, звучные, систолический шум с максимумом на верхушке; артериальное давление 105/69 мм рт. ст. Менингеальные симптомы: не выявлены. Живот при пальпации: мягкий, безболезненный во всех отделах; печень при пальпации не увеличена. Селезенка не увеличена. Стул накануне оформлен. Диурез в норме.
На ЭКГ (рис. 2) — синусовая тахикардия (ЧСС 116 в минуту), АВ-блокада I степени (PQ 0,23 мс).
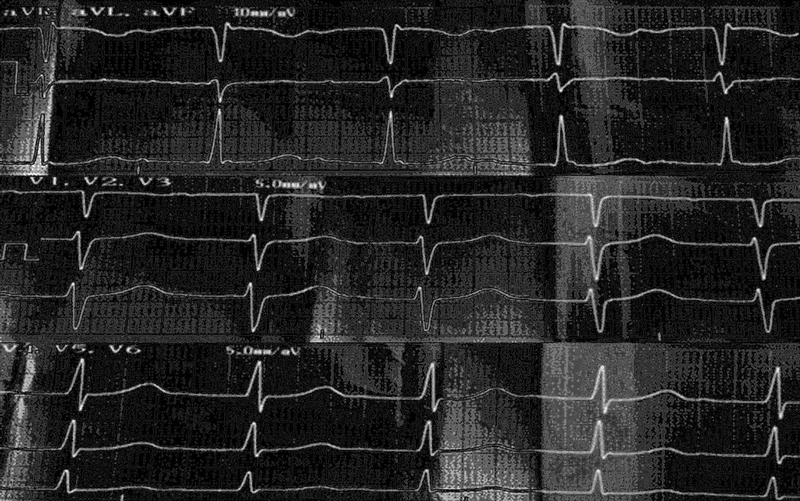
Рис. 2. Фрагмент (усиленные от конечностей, грудные отведения) электрокардиограммы (скорость записи 50 мс) пациента от 11.04 (13-й день болезни)
При проведении эхокардиографии выявлены пролапс митрального клапана 2-й степени (4,2 мм), трикуспидальная регургитация 1-й степени; cократительная способность миокарда в норме.
В гемограмме от 11 апреля — лейкоцитоз 13,5 × 109/л, повышение СОЭ до 40 мм/ч.
Ребенок проконсультирован кардиологом: заподозрен ревмокардит, бактериальный эндокардит. Рекомендовано увеличить дозу цефтриаксона до 75 мг/кг в сутки, добавить в терапии амикацин и пенициллин. С 11 апреля продолжена антибактериальная терапия внутривенно цефтриаксоном в рекомендованной дозе и начата терапия амикацином в дозе 15 мг/кг/сут 3 раза в день. Противовоспалительная терапия проводилась ибупрофеном, метаболическая терапия — кокарбоксилазой, продолжена противовирусная терапия препаратом интерферона в дозе 500 тыс. Ед в день. С 14 апреля начата терапия пенициллином 150 тыс. Ед/кг/сут в/в капельно 4 раза в день. Длительность приема препаратов представлена на рисунке 1.
В ходе терапии отмечалась положительная динамика — к 14 апреля (16-й день болезни) девочка перестала жаловаться на слабость, однако отмечались подъемы температуры до 37,4 °C, тахикардия при аускультации сердца.
В биохимическом анализе от 14 апреля не было выявлено повышения уровня ферментов креатинфосфокиназы (КФК), креатинфосфокиназы-МВ (КФК-МВ) и лактатдегидрогеназы (ЛДГ). Уровень СРБ повысился до 13 мг/л (норма до 5). Уровень К, Na в норме. Уровень АСЛ-О снижался в динамике (см. рис. 1). На ЭКГ сохранялись синусовая тахикардия (ЧСС — 118 ударов в минуту), АВ-блокада I степени.
Самочувствие нормализовалось с 16 апреля (18-й день болезни), температура на нормальных цифрах, жалоб не предъявляла, ЧСС лежа — 80 ударов в минуту, стоя — 106. Артериальное давление на протяжении госпитализации в пределах нормы.
21 апреля (23-й день болезни) ребенок повторно консультирован кардиологом, подтвержден диагноз ревмокардита. Рекомендовано продолжение пенициллинотерапии до 14 дней внутривенно, смена ибупрофена на диклофенак, добавление в терапии эгилока и капотена. В анализе крови от 21 апреля — нормализация СОЭ, числа лейкоцитов, уровня С-реактивного белка. Положительная динамика по ЭКГ в виде нормализации ЧСС, АВ-проведения.
ПЦР от 21 апреля — ДНК ВЭБ в крови не обнаружена.
23 апреля девочка переведена в кардиологическое отделение детской городской больницы, где была продолжена антибактериальная терапия пенициллином. Выписана с выздоровлением 30 апреля (на 32-й день болезни). При выписке нормализация гемограммы, СРБ, АСЛ-О, ЭКГ. При динамическом наблюдении в течение года у пациентки регистрировалась стойкая нормализация состояния, лабораторных показателей. Через год при проведении ЭКГ патологические изменения не выявлены.
Особенностью данного случая является то, что основным симптомом, указывающим на воспалительное поражение миокарда, явилась отрицательная динамика ЭКГ — появление AВ-блокады I степени на фоне синусовой тахикардии, тогда как уровень кардиальных ферментов (КФК-МВ, ЛДГ) оставался нормальным. Связь с перенесенной инфекцией, наличие одного большого (появление патологических изменений на ЭКГ в виде АВ-блокады I степени) и двух малых (лабораторное подтверждение вирусной инфекции Эпштейна – Барр, тахикардия) диагностических критериев миокардита, отсутствие клапанного поражения сердца (основополагающим компонентом ревмокардита считают вальвулит) и других больших диагностических критериев острой ревматической лихорадки (ОРЛ) позволяет исключить ОРЛ и поставить диагноз острого инфекционного (вирусно-бактериального) миокардита, очагового (с преимущественным поражением проводящей системы сердца).
Данный клинический пример подчеркивает важность клинической настороженности в отношении поражения сердца при инфекционных заболеваниях. Появление недомогания, слабости, признаков недостаточности кровообращения, а также патологических ЭКГ-изменений в острый период заболевания или в период реконвалесценции требует проведения комплекса лабораторных и инструментальных исследований для исключения развития патологии сердца, в том числе и миокардита.
About the authors
Anastasiya S Levina
St Petersburg State Pediatric Medical University
Author for correspondence.
Email: rossii@mail.ru
MD, PhD, Assistant Professor. Department of Infectious Diseases in Children, Faculty of Postgraduate Education Russian Federation
Irina V Babachenko
St Petersburg State Pediatric Medical University
Email: babachenko-doc@mail.ru
MD, PhD, Dr Med Sci, Professor. Department of Infectious Diseases in Children, Faculty of Postgraduate Education Russian Federation
Svetlana N Chuprova
Federal Medico-Biological Agency of Russia
Email: svetlana_ch_70@mail.ru
MD, PhD, Senior researcher. Department of Rehabilitation and Regenerative Therapy Russian Federation
Natalia V Kochevaya
Federal Medico-Biological Agency of Russia
Email: natachitarr@mail.ru
Hospital. Research Institute of Children’s Infections Russian Federation
Elena V Sharipova
Federal Medico-Biological Agency of Russia
Email: lenowna2000@yandex.ru
MD, PhD, Researcher. Department of Respiratory (drop) Infections. Research Institute of Children’s Infections Russian Federation
Olesya M Ibragimova
Federal Medico-Biological Agency of Russia
Email: ole_sya_ibr@bk.ru
MD, PhD, Junior researcher. Department of Respiratory (drop) Infections. Research Institute of Children’s Infections Russian Federation
References
- Ивкина С.С., Зарянкина А.И. Неревматические кардиты у детей: учеб.-метод. пособие для студентов медицинских вузов, врачей-интернов, врачей-педиатров, детских кардиологов. — Гомель: ГомГМУ, 2012. [Ivkina SS, Zaryankina AI. Nerevmaticheskie kardity u detey: uchebnoe posobie. Gomel: GomGMU; 2012. (In Russ).]
- Поляков В.П., Николаевский Е.Н., Пичко А.Г. Некоронарогенные и инфекционные заболевания сердца (современные аспекты клиники, диагностики, лечения). — Самара: СамГМУ, 2010. [Polyakov VP, Nikolaevskiy EN, Pichko AG. Nekoronarogennye i infektsionnye zabolevaniya serdtsa (sovremrnnye aspekty kliniki, diagnostiki, lecheniya). Samara: SamGMU; 2010. (In Russ).]
- Самсон А.А., Кишкурно Е.П. Поражение сердечно-сосудистой системы при инфекционных заболеваниях // Медицина неотложных состояний. — 2008. — Т. 1. — № 14. — С. 19–24. [Samson AA, Kishkurno EP. Porazhenie serdechno-sosudistoy sistemy pri infektsionnyh zabolevaniyah. Meditsina neotlozhnyh sostoyaniy. 2008;1(14):19-24. (In Russ).]
- Сторожаков Г.И., Гендлин Г.Е., Тронина О.А. Миокардиты // Сердечная недостаточность. — 2009. — Т. 10. — № 1. — С. 46–52. [Storozhakov GI, Gendlin GE, Tronina OA. Miokardity. Serdechnaya nedostatochnost’. 2009;10(1):46-52. (In Russ).]
- Сторожаков Г.И., Горбаченков А.А., ред. Руководство по кардиологии: учебное пособие: в 3 т. — М.: ГЭОТАР-Медиа, 2008. [Storozhakov GI, Gorbachenkov AA. Rukovodstvo po kardiologii: Uchebnoe posobie. Moscow: GEOTAR-Media; 2008. (In Russ).]
- Толстикова Т.В., Брегаль Л.В. Осложнения инфекционного мононуклеоза и Эпштейна — Барр вирусной инфекции // Тюмен. мед. журн. —2005. — № 3. — С. 15–17. [Tolstikova TV, Bregal’ LV. Oslozhneniya infektsionnogo mononukleoza I Epshteyna-Barr virusnoy infektsii. Tumenskiy meditsinskiy zhurnal. 2005;(3):15-17. (In Russ).]
- Шляхто Е.В., ред. Рекомендации РНМОТ и ОССН по диагностике и лечению миокардитов. — М., 2012. [Shlyahto EV, ed. Rekomendatsii RNMOT I OSSN po diagnostike I lecheniyu miokarditov. Moscow; 2012. (In Russ).]
- Шостак Н.А., Аксенова А.В., Константинова Е.В., Клименко А.А. Диагностика и лечение неревматических миокардитов (40-летний опыт изучения) // Вестник Российского государственного медицинского университета. — 2009. — № 7. — С. 102–106. [Shostak NA, Aksenova AV, Konstantinova EV, Klimenko AA. Diagnostika I lechenie nerevmaticheskih miokarditov (40-letniy opyt izucheniya). Vestnik Rossiyskogo gosudarstvennogo universiteta. 2009;7:102-106. (In Russ).]
- Dennert R, Crijns HL, Heymans S. Acute viral myocarditis. Eur Heart J. 2008;29:2073-2082. doi: 10.1093/eurheartj/ehn296.
Supplementary files







