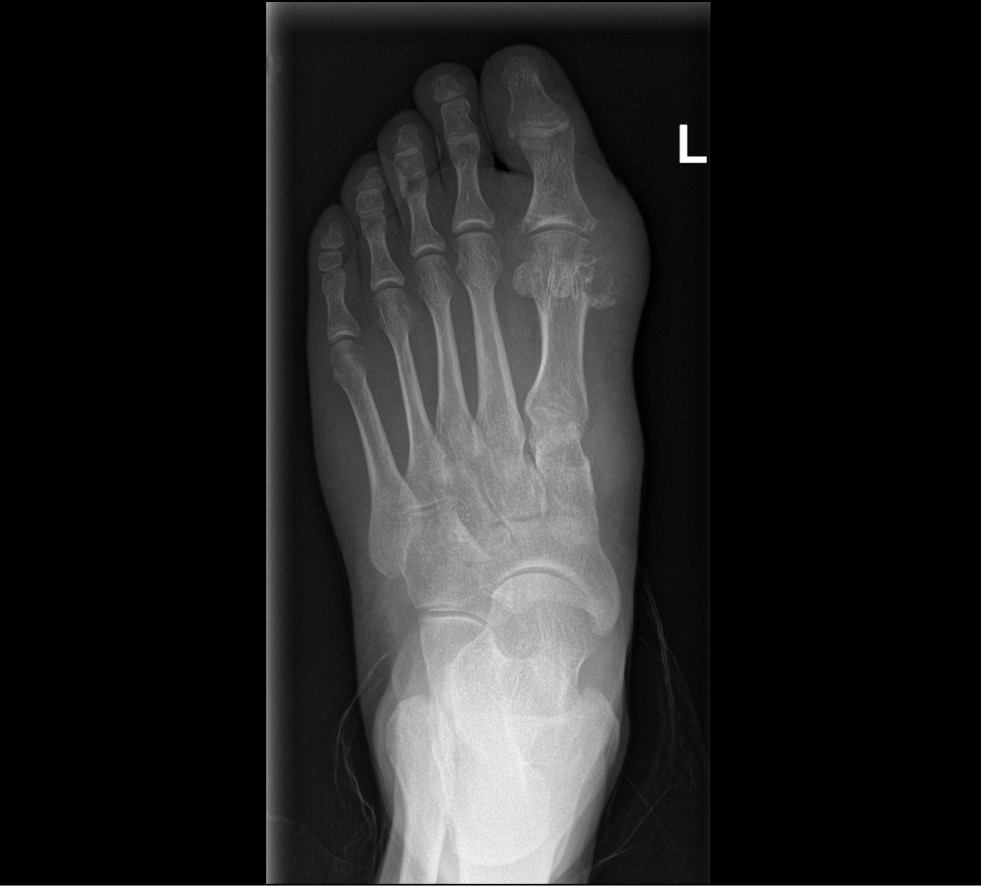
双能量计算机断层扫描在诊断痛风和其他结晶性关节病中的作用:文献综述
- 作者: Onoyko M.V.1, Mershina E.A.1, Georginova O.A.1, Plotnikova M.L.1, Panyukova A.V.1, Sinitsyn V.E.1
-
隶属关系:
- Lomonosov Moscow State University
- 期: 卷 4, 编号 2 (2023)
- 页面: 197-213
- 栏目: 科学评论
- URL: https://journals.rcsi.science/DD/article/view/146886
- DOI: https://doi.org/10.17816/DD322758
- ID: 146886
如何引用文章
详细
本文讨论了双能量计算机断层扫描的操作原理、其诊断准确性以及最常见的伪影类型。考虑了在双能量计算机断层扫描过程中,单钠尿酸盐沉积的存在对其他临床数据的可能依赖性,双能量计算机断层扫描在诊断痛风中的意义以及其在结晶性关节病的鉴别诊断中的作用。
与作为诊断痛风金标准的诊断性关节穿刺术相比,双能量计算机断层扫描有几个优点:无创性、执行速度、医源性并发症风险的多次减少。痛风的检测、治疗效果的监测、鉴别诊断的可能性,都是可以通过双能量计算机断层扫描来实现的。
作者简介
Maria V. Onoyko
Lomonosov Moscow State University
Email: onoykomary@gmail.com
ORCID iD: 0000-0002-7727-3360
俄罗斯联邦, Moscow
Elena A. Mershina
Lomonosov Moscow State University
Email: elena_mershina@mail.ru
ORCID iD: 0000-0002-1266-4926
SPIN 代码: 6897-9641
MD, Cand. Sci. (Med), Associate Professor
俄罗斯联邦, MoscowOlga A. Georginova
Lomonosov Moscow State University
Email: olga.georginova@gmail.com
ORCID iD: 0000-0002-7542-8189
SPIN 代码: 8331-3656
MD, Cand. Sci. (Med), Assistant Professor
俄罗斯联邦, MoscowMaria L. Plotnikova
Lomonosov Moscow State University
Email: maria_plotnikova@inbox.ru
ORCID iD: 0000-0001-7533-9867
俄罗斯联邦, Moscow
Alexandra V. Panyukova
Lomonosov Moscow State University
Email: panyukovaalexandra@gmail.com
ORCID iD: 0000-0002-5367-280X
俄罗斯联邦, Moscow
Valentin E. Sinitsyn
Lomonosov Moscow State University
编辑信件的主要联系方式.
Email: vsini@mail.ru
ORCID iD: 0000-0002-5649-2193
SPIN 代码: 8449-6590
MD, PhD, Professor, Medical Research and Educational Center
俄罗斯联邦, Moscow参考
- Neogi T, Jansen TL, Dalbeth N, et al. 2015 Gout classification criteria: An American college of rheumatology / European league against rheumatism collaborative initiative. Arthritis Rheumatol. 2015;67(10):2557–2568. doi: 10.1002/art.39254
- Taylor WJ, Fransen J, Dalbeth N, et al. Diagnostic arthrocentesis for suspicion of gout is safe and well tolerated. J Rheumatol. 2016;43(1):150–153. doi: 10.3899/jrheum.150684
- Sikilinda V, Alabut A. Protocols of technique of punctions of joints and treatment blocades in trauma and orthopedic diseases of support-moving apparatus. Chief Physician South Russia. 2018;2 (60):14–20. (In Russ).
- Stauder SK, Peloso PM. Dual-Energy computed tomography has additional prognostic value over clinical measures in gout including tophi: A systematic literature review. J Rheumatol. 2022;49(11):1256–1268. doi: 10.3899/jrheum.211246
- Federal Clinical Guidelines. Gout. All-Russian Public Organization Association of Rheumatologists of Russia; 2014. (In Russ).
- Dalbeth N, Phipps-Green A, Frampton C, et al. Relationship between serum urate concentration and clinically evident incident gout: An individual participant data analysis. Ann Rheum Dis. 2018;77(7):1048–1052. doi: 10.1136/annrheumdis-2017-212288
- Pereverzev AP, Ostroumova OD. Drug-induced hyperuricemia/gout. Part I: Prevalence, pathophysiology, risk factors, clinical pattern. Therapy. 2021;7(6):136–145. (In Russ). doi: 10.18565/therapy.2021.7.159-169
- Chhana A, Lee G, Dalbeth N. Factors influencing the crystallization of monosodium urate: A systematic literature review. BMC Musculoskelet Disord. 2015;16(1):1–11. doi: 10.1186/s12891-015-0762-4
- Fiddis RW, Vlachos N, Calvert PD. Studies of urate crystallisation in relation to gout. Ann Rheum Dis. 1983;42(Suppl 1):12. doi: 10.1136/ard.42.suppl_1.12
- Dalbeth N, Pool B, Gamble GD, et al. Cellular characterization of the gouty tophus: A quantitative analysis. Arthritis Rheum. 2010;62(5):1549–1556. doi: 10.1002/art.27356
- Butler F, Alghubayshi A, Roman Y. The epidemiology and genetics of hyperuricemia and gout across major racial groups: A literature review and population genetics secondary database analysis. J Personalized Med. 2021;11(3):231. doi: 10.3390/jpm11030231
- Meneses-Leon J, Denova-Gutiérrez E, Castañón-Robles S, et al. Sweetened beverage consumption and the risk of hyperuricemia in Mexican adults: A cross-sectional study. BMC Public Health. 2014;14(1):1–11. doi: 10.1186/1471-2458-14-445
- Bae J, Chun BY, Park PS, et al. Higher consumption of sugar-sweetened soft drinks increases the risk of hyperuricemia in Korean population: The Korean multi-rural communities cohort study. Semin Arthritis Rheum. 2014;43(5):654–661. doi: 10.1016/j.semarthrit.2013.10.008
- Zhang W, Doherty M, Pascual E, et al. EULAR evidence based recommendations for gout. Part I: Diagnosis. Report of a task force of the standing committee for international clinical studies including therapeutics (ESCISIT). Ann Rheum Dis. 2006;65(10):1301–1311. doi: 10.1136/ard.2006.055251
- Kienhorst LB, Janssens HJ, Eijgelaar RS, et al. The detection of monosodium urate crystals in synovial fluid after long-term and varying storage conditions. Joint Bone Spine. 2015;82(6):470–471. doi: 10.1016/j.jbspin.2014.10.020
- Secrets of rheumatology. Ed. by S.D. West. Trans. from English ed. by O.M. Lesnyak. Moscow: GEOTAR-Media; 2021. 756 p. (In Russ).
- Malik A, Schumacher HR, Dinnella JE, Clayburne GM. Clinical diagnostic criteria for gout: Comparsion with the gold standard of synovial fluid crystal analysis. J Clin Rheumatol. 2009;15(1):22–24. doi: 10.1097/RHU.0b013e3181945b79
- Pascal Z, Valcov R, Fabreguet I, et al. A prospective evaluation of ultrasound as a diagnostic tool in acute microcrystalline arthritis. Arthritis Res Ther. 2015;17(1):1–8. doi: 10.1186/s13075-015-0701-7
- Omoumi P, Becce F, Racine D, et al. Basic principles, technical approaches, and applications in musculoskeletal imaging (Part I). Semin Musculoskelet Radiol. 2015;19(5):431–437. doi: 10.1055/s-0035-1569253
- Ogdie A, Taylor WJ, Weatherall M, et al. Imaging modalities for the classification of gout: systematic literature review and meta-analysis. Ann Rheum Dis. 2015;74(10):1868–1874. doi: 10.1136/annrheumdis-2014-205431
- Sapsford M, Gamble GD, Aati O, et al. Relationship of bone erosion with the urate and soft tissue components of the tophus in gout: A dual energy computed tomography study. Rheumatology (Oxford). 2017;56(1):129–133. doi: 10.1093/rheumatology/kew383
- Towiwat P, Doyle AJ, Gamble GD, et al. Urate crystal deposition and bone erosion in gout: “Inside-out” or “outside-in”? A dual-energy computed tomography study. Arthritis Res Ther. 2016;18(1):208. doi: 10.1186/s13075-016-1105-z
- Bayat S, Aati O, Rech J, et al. Development of a dual-energy computed tomography scoring system for measurement of urate deposition in gout. Arthritis Care Res (Hoboken). 2016;68(6):769–775. doi: 10.1002/acr.22754
- Rajiah P, Sundaram M, Subhas N. Dual-energy CT in musculoskeletal imaging: What is the role beyond gout? AJR Am J Roentgenol. 2019;213(3):493–505. doi: 10.2214/AJR.19.21095
- Klimkova MM, Sinitsyn VE, Mazurenko DA, et al. Perspectives of dual-energy computed tomography in diagnostic of urinary stone disease for the determination of urinary calculi composition (review). Med Visualization. 2016;(6):84–92. (In Russ).
- McCollough CH, Leng S, Yu L, Fletcher JG. Dual- and multi-energy CT: Principles, technical approaches, and clinical applications. Radiology. 2015;276(3):637–653. doi: 10.1148/radiol.2015142631
- Sodickson AD, Keraliya A, Czakowski B, et al. Dual energy CT in clinical routine: How it works and how it adds value. Emerg Radiol. 2021;28(1):103–117. doi: 10.1007/s10140-020-01785-2
- Megibow AJ, Kambadakone A, Ananthakrishnan L. Dual-energy computed tomography: Image acquisition, processing, and workflow. Radiol Clin North Am. 2018;56(4):507–520. doi: 10.1016/j.rcl.2018.03.001
- Forghani R, De Man B, Gupta R. Dual-energy computed tomography: Physical principles, approaches to scanning, usage, and implementation: Part 2. Neuroimaging Clin N Am. 2017;27(3):385–400. doi: 10.1016/j.nic.2017.03.002
- Henzler T, Fink C, Schoenberg SO, et al. Radiation dose aspects. AJR Am J Roentgenol. 2012;199(5 Suppl):S16–S25. doi: 10.2214/AJR.12.9210
- Borges AP, Antunes C, Curvo-Semedo L. Pros and cons of dual-energy CT systems: “One does not fit all”. Tomography. 2023;9(1):195–216. doi: 10.3390/tomography9010017
- Parakh A, Lennartz S, An C, et al. Dual-energy CT images: Pearls and pitfalls. Radiographics. 2021;41(1):98–119. doi: 10.1148/rg.2021200102
- Gosangi B, Mandell MC, Weaver MJ, et al. Bone marrow edema at dual-energy CT: A game changer in the emergency department. Radiographics. 2020;40(3):859–874. doi: 10.1148/rg.2020190173
- Goo HW, Goo JM. Dual-energy CT. New horizon in medical imaging. Korean J Radiol. 2017;18(4):555–569. doi: 10.3348/kjr.2017.18.4.555
- Baer AN, Kurano T, Thakur UJ, et al. Dual-energy computed tomography has limited sensitivity for non-tophaceous gout: A comparison study with tophaceous gout. BMC Musculoskelet Disord. 2016;17(1):1–9. doi: 10.1186/s12891-016-0943-9
- Bongartz T, Glazebrook KN, Kavros SJ, et al. Dual-energy CT for the diagnosis of gout: an accuracy and diagnostic yield study. Ann Rheum Dis. 2015;74(6):1072–1077. doi: 10.1136/annrheumdis-2013-205095
- Huppertz A, Hermann A, Diekhoff T, et al. Systemic staging for urate crystal deposits with dual-energy CT and ultrasound in patients with suspected gout. Rheumatol Int. 2014;(3):763–771. doi: 10.1007/s00296-014-2979-1
- Strobl S, Halpern EJ, Abd Ellah M, et al. Acute gouty knee arthritis: Ultrasound findings compared with dual-energy CT findings. AJR Am J Roentgenol. 2018;210(6):1323–1329. doi: 10.2214/AJR.17.19199
- Mallinson PI, Coupal T, Reisinger C, et al. Artifacts in dual-energy CT gout protocol: A review of 50 suspected cases with an artifact identification guide. AJR Am J Roentgenol. 2014;203(1):103–109. doi: 10.2214/AJR.13.11396
- Omoumi P, Zufferey P, Malghem J, So A. Imaging in gout and other crystal-related arthropathies. Rheum Dis Clin North Am. 2016;42(4):624–644. doi: 10.1016/j.rdc.2016.07.005
- Lee SM, Lee JG, Lee G, et al. CT Image conversion among different reconstruction kernels without a sinogram by using a convolutional neural network. Korean J Radiol. 2019;20(2):295–303. doi: 10.3348/kjr.2018.0249
- Alavandar E, Arunachalam VK, Narappulan N, et al. Principles and available hardware in DECT. J Gastrointestinal Abdominal Radiology. 2022;5(6). doi: 10.1055/s-0042-1742772
- Lee JS, Seo WJ. What is the diagnostic value of dual-energy computed tomography in patients with clinical diagnosis of gout? Adv Rheumatol. 2021;61(1):1–7. doi: 10.1186/s42358-021-00198-0
- Jia E, Zhu J, Huang W, et al. Dual-energy computed tomography has limited diagnostic sensitivity for short-term gout. Clin Rheumatol. 2018;37(3):773–777. doi: 10.1007/s10067-017-3753-z
- Ramon A, Ornetti P. Dual energy computed tomography: A breakthrough for gout? Joint Bone Spine. 2020;87(4):289–291. doi: 10.1016/j.jbspin.2019.12.002
- Shang J, Li XH, Lu SQ, et al. Gout of feet and ankles in different disease durations: Diagnostic value of single-source DECT and evaluation of urate deposition with a novel semi-quantitative DECT scoring system. Adv Rheumatol. 2021;61(1):1–14. doi: 10.1186/s42358-021-00194-4
- Wang P, Smith SE, Garg R, et al. Identification of monosodium urate crystal deposits in patients with asymptomatic hyperuricemia using dual-energy CT. RMD Open. 2018;4(1):593–597. doi: 10.1136/rmdopen-2017-000593
- Urano W, Yamanaka H, Tsutani H, et al. The inflammatory process in the mechanism of decreased serum uric acid concentrations during acute gouty arthritis. J Rheumatol. 2002;29(9):1950–1953.
- Dalbeth N, Nicolaou S, Baumgartner S, et al. Presence of monosodium urate crystal deposition by dual-energy CT in patients with gout treated with allopurinol. Ann Rheum Dis. 2018;77(3):364–370. doi: 10.1136/annrheumdis-2017-212046
- Zhang W, Doherty M, Bardin T, et al. European league against rheumatism recommendations for calcium pyrophosphate deposition. Part I: Terminology and diagnosis. Ann Rheum Dis. 2011;70(4):563–570. doi: 10.1136/ard.2010.139105
- Sabchyshyn V, Konon I, Ryan LM, Rosenthal AK. Concurrence of rheumatoid arthritis and calcium pyrophosphate deposition disease: A case collection and review of the literature. Semin Arthritis Rheum. 2018;48(1):9–11. doi: 10.1016/j.semarthrit.2017.11.009
- Williams CJ, Rosenthal AK. Pathogenesis of calcium pyrophosphate deposition disease. Best Pract Res Clin Rheumatol. 2021;35(4):101718. doi: 10.1016/j.berh.2021.101718
- Abhishek A. Calcium pyrophosphate deposition. Br J Hosp Med (Lond). 2014;75(4):61–64. doi: 10.12968/hmed.2014.75.sup4.c61
- Miksanek J, Rosenthal AK. Imaging of calcium pyrophosphate deposition disease. Curr Rheumatol Rep. 2015;17(3):20. doi: 10.1007/s11926-015-0496-1
- Godfrin-Valnet M, Godfrin G, Godard J, et al. Eighteen cases of crowned dens syndrome: Presentation and diagnosis. Neurochirurgie. 2013;59(3):115–120. doi: 10.1016/j.neuchi.2013.03.003
- Cipolletta E, Filippou G, Scirè CA, et al. The diagnostic value of conventional radiography and musculoskeletal ultrasonography in calcium pyrophosphate deposition disease: a systematic literature review and meta-analysis. Osteoarthr Cartil. 2021;29(5):619–632. doi: 10.1016/j.joca.2021.01.007
- Lee KA, Lee SH, Kim HR. Diagnostic value of ultrasound in calcium pyrophosphate deposition disease of the knee joint. Osteoarthr Cartil. 2019;27(5):781–787. doi: 10.1016/j.joca.2018.11.013
- Neame RL, Carr AJ, Muir K, Doherty M. UK community prevalence of knee chondrocalcinosis: Evidence that correlation with osteoarthritis is through a shared association with osteophyte. Ann Rheum Dis. 2003;62(6):513–518. doi: 10.1136/ard.62.6.513
- Frediani B, Filippou G, Falsetti P, et al. Diagnosis of calcium pyrophosphate dihydrate crystal deposition disease: Ultrasonographic criteria proposed. Ann Rheum Dis. 2005;64(4):638–640. doi: 10.1136/ard.2004.024109
- Tanikawa H, Ogawa R, Okuma K, et al. Detection of calcium pyrophosphate dihydrate crystals in knee meniscus by dual-energy computed tomography. J Orthop Surg Res. 2018;13(1):73. doi: 10.1186/s13018-018-0787-0
- Rosales-Alexander JL, Aznar JB, Magro-Checa C. Calcium pyrophosphate crystal deposition disease: Diagnosis and treatment. Open Access Rheumatol. 2014;(6):39–47. doi: 10.2147/OARRR.S39039
- Sekijima Y, Yoshida T, Ikeda SI. CPPD crystal deposition disease of the cervical spine: A common cause of acute neck pain encountered in the neurology department. J Neurol Sci. 2010;296(1–2):79–82. doi: 10.1016/j.jns.2010.05.028
- Kravchenko D, Karakostas P, Kuetting D, et al. The role of dual energy computed tomography in the differentiation of acute gout flares and acute calcium pyrophosphate crystal arthritis. Clin Rheumatol. 2022;41(1):223–233. doi: 10.1007/s10067-021-05949-4
- Tedeschi SK, Solomon DH, Yoshida K, et al. A prospective study of dual-energy CT scanning, US and X-ray in acute calcium pyrophosphate crystal arthritis. Rheumatology (Oxford). 2020;59(4):900–903. doi: 10.1093/rheumatology/kez431
- Pascart T, Norberciak L, Legrand J, et al. Dual-energy computed tomography in calcium pyrophosphate deposition: Initial clinical experience. Osteoarthr Cartil. 2019;27(9):1309–1314. doi: 10.1016/j.joca.2019.05.007
补充文件